UČNI NAČRT PREDMETA / COURSE SYLLABUS. Predmet: ANALIZNA KEMIJA 3 Course Title: ANALYTICAL CHEMISTRY 3
|
|
|
- Sabrina Conley
- 5 years ago
- Views:
Transcription
1 doc. dr. Mitja Kolar FKKT ULJ, kabinet 2100, govorilne ure sreda med 10 in 12h UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: ANALIZNA KEMIJA 3 Course Title: ANALYTICAL CHEMISTRY 3 Study Programme and Level Študijska smer Letnik Semester VSŠP Kemijska tehnologija, 1. stopnja / PSP Chemical Technology, 1 st Cycle / 3 rd 5 th Vrsta predmeta / Course Type: obvezni / Mandatory Univerzitetna koda predmeta / University Course Code: KT131 Predavanja Seminar Vaje Druge oblike študija Samost. delo ECTS LV / / 75 5 Nosilec predmeta / Lecturer: izr. prof. dr. Nataša Gros, doc. dr. Mitja Kolar Jeziki / Languages: Predavanja / Lectures: slovenski / Slovenian Vaje / Tutorial: slovenski / Slovenian Pogoji za vključitev v delo oz. za opravljanje študijskih obveznosti: Študent oz. kandidat mora imeti predmet opredeljen kot študijsko obveznost. Prerequisites: The course has to be assigned to the student. Vsebina: Temelji kromatografije in delitev kromatografskih tehnik. Tekočinska kromatografija visoke ločljivosti (enote HPLC sistema, vrste polnitev kolon, normalno fazna, reverzno fazna, velikostno izključitvena kromatografija, vrste detektorjev, analizne aplikacije). Ionska kromatografija (delitve ionske kromatografije, enote ionskega kromatografa, polnitve kolon, analizne aplikacije). Tenkoplastna kromatografija (temeljni pojmi in izvedbe, identifikacija in kvantifikacija ločenih komponent, analizne aplikacije). Plinska kromatografija (enote plinskega kromatografa, različne izvedbe injektorjev, vrste kolon, detektorji, analizne aplikacije). Kapilarna elektroforeza (elektroforezne tehnike, elektro osmotski tok, elektroferogram, analizne aplikacije). Sklopitve kromatografskih tehnik z masnim spektrometrom. 1
2 Vsebina: Prikaz, vrednotenje in interpretacija analiznih rezultatov. Box and Whisker graf, histogramski in poligonski prikazi, test normalne porazdelitve Interval zaupanja in statistični testi (F test, različne izvedbe t testa, Q test) Uporaba linearne regresije za primerjavo rezultatov dveh metod. Vaje nadgradijo in razširijo nabor instrumentalnih analiznih metod, ki so jih študentje uporabljali pri vajah v drugem letniku in vključijo dodatne vidike vrednotenja in interpretacije rezultatov. Content (Syllabus outline): Separation methods: Fundamentals of chromatography, different chromatographic methods an overview. High performance liquid chromatography (HPLC system, chromatographic columns, different techniques in HPLC, detection, analytical applications). Ion chromatography (classification in ion chromatography, ion chromatographic systems, chromatographic columns, analytical applications). Thin layer chromatography (terminology, designs, identification and quantification, analytical applications). Gas chromatography (instrumentation, columns, detectors, analytical applications). Capillary electrophoresis (techniques, electroosmotic flow, electroferogram, analytical applications). Hyphenation of chromatographic techniques with mass spectrometry. Presentation, evaluation and interpretation of analytical results Box and Whisker graph, histogram, polygon, test of normal distribution Confidence interval, statistical tests (F test, t-test,q test) Use of linear regression for a comparison of the results of two analytical methods. Laboratory class: Instrumental analytical methods and evaluation and interpretation of results. Izbrana oz. posamezna poglavja iz: Francis, Rouessac, Annick Rouessac, Chemical Analysis Modern Instrumental Methods, Wiley, 2000, Chichester. Or later editions. Chapters 1 to 5 and pages. James N. Miller, Jane C. Miller, Statistics and Chemometrics for Analytical Chemistry, 6th Edition, Pearson Education, 2010, Harlow. Chapters 2, 3, 5.10, pages. V navedenih učbenikih so tudi rešeni računski primeri in naloge! 2
3 Dodatni viri Fundamentals of Analytical Chemistry, D.A.Skoog, F.J. Holler, T.A. Nieman, Thomson Learning ARC-Brooks/Cole, Gary D. Christian, Analytical Chemistry, Willey, 5th edition. Analytical Chemistry, G.D. Christian, P.K. Dasgupta, K.A. Schug, Wiley Modern Practise of Gas Chromatography, R. L. Grob, E. F. Barry, Wiley, Encyclopedia of Chromatography, J. Cazes, Marcel Dekker, Kemometija in obdelava eksperimentalnih podatkov, J. Zupan, Inštitut nove revije, Zavod za humanistiko in Kemijski inštitut Ljubljana, Cilji in kompetence: Pri predmetu študent študent pridobi znanja o separacijskih analiznih metodah. Pri vajah se usposobi za praktično izvedbo dodatnega nabora instrumentalnih analiznih metod. Zmožnost predstavitve,vrednotenja in interpretacije rezultatov osvojene v drugem letniku študent razširi z dodatnimi statističnimi prijemi. Objectives and Competences: Understanding and knowledge of separation methods. Experimental skills and ability of using instrumental analytical methods. Upgraded knowledge in interpretation and evaluation of analytical results. Predvideni študijski rezultati / Intended Learning Outcomes: Znanje in razumevanje Študent razume temelje in uporabo obravnavanih analiznih metod. Študent osvoji dodatna znanja za predstavitev, vrednotenje in interpretacijo analiznih rezultatov. Knowledge and Comprehension Student fosters understanding of fundamentals and applications of analytical methods. Ability of evaluating, presenting and interpreting analytical results. Uporaba Študent zna izvesti analizne postopke in meritve vezane na obravnavane analizne metode ter ovrednotiti dobljene rezultate. Application Student is able to perform analyses and evaluate analytical results. Refleksija Študent je kritičen do dobljenih rezultatov in se zaveda omejitev analiznih metod. Analysis Student develops a critical attitude towards analytical result and is aware of the limitation of analytical methods. Prenosljive spretnosti Laboratorijske spretnosti, statistično vrednotenje in interpretacija rezultatov. Skill-transference Ability Laboratory skills, statistical methods, interpretation of analytical results. Metode poučevanja in učenja / Learning and Teaching Methods: Predavanja, vodeni razgovor, sodelovalno učenje, reševanje problemov. Lectures, guided discussions, cooperative learning, problem solving. 3
4 Načini ocenjevanja: Delež (v %) Končna ocena: Vaje 33,3 % Izpit 66,7 % Vaje: Esej:»Ovrednotenje kakovosti naravne vode«. Predmet: Pisni izpit. Predpogoj za izpit so uspešno zaključene vaje. Več informacij o poteku študijskega programa z opisi predmetov najdete na pod: doc. dr. Mitja Kolar 4
5 Identifikacija in določanje organskih spojin Sočasno določanje več organskih spojin Kromatografija: ločevanje spojin identifikacija-kvalitativna kvantitativna analiza Kromatografija Interakcija med molekulami topljenca in stacionarno fazofizikalni procesi topilo mobilna faza topilo Kromatografske metode delimo: glede na prevladujočo interakcijo, - porazdelitev, - ionska izmenjava, - adsorpcija, - izključitev Cvet ločil listna barvila na koloni iz CaCO 3 topilo petrolej Ismailov, Shraiber začetki papirne in tankoplastne kromatografije eluent Stacionarna faza ločene komponente v mobilni fazi glede na agregatno stanje mobilne faze, - tekoča, - plinasta, - superkritični fluid npr. CO 2, glede na lego, vrsto in nanos stacionarne faze, 1952 plinska kromatografija glede na način izvedbe: - preparativno delo, - analitsko delo. 5
6 Princip kromatografskih separacij Porazdelitvena kromatografija (topljenci se porazdelijo med dve topili, ki se ne mešata) Adsorptivna kromatografija (topljenci se različno adsorbirajo na površino trdnega adsorbenta) Velikostno izključitvena kromatografija (ločevanje na osnovi velikosti molekul; makromolekule-polimeri, proteini ) Ionska izmenjava (ločevanje nabitih zvrsti npr. kationov, anionov) Kolonska kromatografija, tankoplastna kromatografija Princip kromatografskih separacij porazdelitev adsorpcija izključitev ionska izmenjava s c s Porazdelitvene/adsorpcijske izoterme A B A mobilna faza Start kromatografska pot konec B c m Spojine se različno porazdeljujejo med dve fazi zaradi različnih K K = c s /c m (porazdelitveni ali adsorpcijski koeficient) Linearno Nelinearno področje izoterm Vpliv na K? Večja interakcija s stacionarno/mobilno fazo 6
7 Delitev kromatografskih metod Delitev glede na lego, vrsto in nanos stacionarne faze: - stacionarna faza je v koloni-kolonska kromatografija (GC, HPLC) - instrumentalne metode - stacionarna faza je nanešena v tanki plasti-tankoplastna kromatografija - delno avtomatizirane Delitev kromatografskih metod 1. Agregatno stanje mobilne faze: plin GC; tekoče HPLC, SF PLIN TEKOČA (porazdelitev) (GLC) PLINSKA (GC) PLIN-TRDNA (adsorpcija) (GSC) KROMATOGRAFIJA TEKOČINSAKA (LC) Tekoča-tekoča Tekoča -trdna Tekoča-trdna Tekoča-trdna (porazdelitev) (adsorpcija) (ionska izmenjava) (izločitev) (LLC) (LSC) (IEC) (EC) Kromatografska ločba pri tankoplastni kromatografiji 2. Princip ločevanja: adsorpcija, porazdelitev Mobilna faza potuje zaradi kapilarnih sil med porami delcev velikosti Angströmov. Spojine so raztopljene v mobilni fazi in potujejo do določene razdalje. Zaradi različnega razmerja med adsorpcijo in / ali porazdelitvijo je čas zadrževanja spojin v stacionarni fazi različen. (PC, TLC) 7
8 fronta A Tankoplastna in papirna kromatografija B s c Retardacijski - retencijski faktor R f kvalitativna analiza R f = pot analita v (mm) / pot topila (mm) R f je odvisen od eksperimentalnih pogojev, zato ga primerjamo z R f standarda R A = a/c a = pot analita A v (mm) c = pot topila v (mm) Plošče z nanešenim sorbentom (stac.f.) Izbor: različni tipi sorbenta na različnih nosilcih v različnih velikostih Vrste sorbentov: splošno uporabni in posebni za določene probleme Sorbenti-stacionarna faza Silikageli (90% aplikacij!) Aluminijev oksid RP- plasti (RP-2, RP-8, RP-18) Amino-, ciano- in diol faze Poliamidi Celuloze Kieselguhr Impregnirane plasti Plasti za ionsko izmenjavo start a R B = s/c Sledi: R AB = R A /R B = a/s s = pot analita B v (mm) c = pot topila v (mm) Nosilci: steklo (za neposredno vrednotenje kromatogramov) plastična folija, aluminijasta folija (cenejši, lahko se režejo s škarjami) Polarnost sorbenta: Polarne stacionarne faze zadržujejo polarne spojine Si > NH 2 > CN / Diol > RP-2 > RP-8 > RP-18 8
9 Kapilarne tehnike Enkratno razvijanje vertikalno Razvijanje plošč Enodimenzionalno razvijanje cirkularno horizontalno antiparalelno anticirkularno Kadi za razvijanje Detekcija spojin na ploščah Ločevanje obarvanih spojin: na plošči vidimo po razvijanju različne barvne lise. Kad s prekatom Ločevanje brezbarvnih spojin: ploščo po razvijanju orosimo z različnimi reagenti, ki tvorijo obarvane produkte. Dvodimenzionalno razvijanje 2 2 Forced flow tehnike OPLC RPC, HPPLC p p Opazovanje plošče po razvijanju pod UV svetloboza spojine, ki absorbirajo svetlobo. 1 1 Normalna kad Horizontalna kad Slike: CAMAG 9
10 VIS VIS 254 nm 366 nm 366 nm 10
11 Kvantitativna analiza Liso s spojino odpraskamo s plošče, jo raztopimo v primernem topilu in določimo spektrofotometrično. Na ploščo nanašamo različne množine spojine in primerjamo velikost lis. Denzitometrija: S posebno opremo izmerimo velikostintentiteto lise, dobimo zapis v obliki kromatogama. Področja uporabe TLC Uporaba za klinične preiskave: Lipidi Študij metabolizma (prirojene okvare, L/M test) Doping kontrola Uporaba za preiskave v industriji Razvijanje in optimizacija proizvodnih procesov Monitoring proizvodnih procesov Validacije čiščenja Prehrana in živalska krma: Kontrola kvalitete Aditivi (npr. vitamini) Pesticidi Testiranje stabilnosti (rok uporabe) Vir: CAMAG Področja uporabe TLC (nadaljevanje) V farmacevtiki: Kontrola kvalitete Identifikacija in kontrola čistote Preverjanje stabilnosti Izolacija biološko aktivnih spojin iz rastlinskih materialov Forenzične preiskave: Detektiranje ponarejenih dokumentov Raziskave zastrupitev Analiza barvil Okolje: Voda Zemlja Analize ostankov Vir: CAMAG 11
12 Papirna kromatografija Stacionarna faza je celuloza Princip ločevanja je adsorpcija in porazdelitev Poceni Filter papir manj stabilen, zato celulozo nanesejo na nosilec in se potem uporablja kot TLC Kolonske kromatografije - stacionarna faza je v koloni Kako in zakaj se spojine ločujejo na kromatografski koloni? 1 nosilni plin 2 nosilni plin 3 nosilni plin 12
13 signal Rezultat kromatografske analize = kromatogram Iz kromatograma določimo število spojin v mešanici, identificiramo spojine in jih kvantitativno določimo. vbrizg t 0 ali V 0 t r ali V r A B čas (min) ali volumen W C h Kromatografski parametri - kromatogram Retencijski čas t r uporabimo za identifikacijo, primerjamo ga s t r znane spojine (standarda) Mrtvi čas t m čas, ki je potreben za zamenjavo mobilne faze v koloni Korigiran retencijski čas Mrtvi volumen V m Retencijski volumen V r Kromatografski parametri retencijski čas Retencijski čas (t r ) je čas, ki ga določena spojina potrebuje, da se pri izbranih pogojih eluira skozi kolono. To je čas, ko se komponenta zadržuje v koloni ter je konstanten za vsako spojino pri določenih kromatografskih pogojih, kot so dimenzija kolone, tip stacionarne faze, pretok in vrsta mobilne faze, velikost delcev v koloni in temperatura. Da sta dve komponenti ločeni, se morata njuna retencijska časa razlikovati. Retencijski čas sestavljata dva dela; čas, ki ga spojina prebije v mobilni fazi (t m ) ter čas, ko se nahaja na stacionarni fazi (retencijski čas t' r ): t r = t m + t r 13
14 Kromatografski parametri porazdelitveni koeficient K D Vsaka komponenta analit A, ki jo nanesemo na stacionarno fazo je pod vplivom procesov sorpcije in desorpcije. Porazdelitev med stacionarno fazo SF in mobilno fazo MF opišemo kot porazdelitev: A m A s K D = [A s ] / [A m ] kjer je K D porazdelitveni termodinamski koeficient za analit A. Višje vrednosti K D pomenijo, da se analit bolj zadržuje v SF in posledično počasneje potuje skozi kolono! Koncept števila teoretskih podov Število teoretskih podov (N) je privzeto iz teorije destilacije (frakcionirna destilacija), pri kateri privzamemo, da je kolona za takšno destilacijo sestavljena iz velikega števila podov ali platojev, kjer je vzpostavljeno ravnotežje med fazama: N = L H N predstavlja potencialno zmožnost kolone za separacijo, večji kot je N večja je učinkovitost. N je proporcionalen z dolžino kolone, zato lahko s primerjavo H - višino poda, primerjamo učinkovitost različno dolgih kolon. Kromatografski parametri - število teoretskih podov Število teoretskih podov (N) je merilo učinkovitosti kolone. Definirano je kot razmerje med dolžino kolone (L) in višino poda (H), kar prikazuje enačba: N = L H Učinkovitost kolone narašča, ko se višina poda zmanjšuje. Število teoretskih podov lahko določimo iz kromatograma z merjenjem retencijskega časa spojine in širine vrha pri bazni liniji: N = 16 ( t r w )2 Boljše rezultate dobimo, če namesto širine vrha pri bazni liniji uporabimo širino vrha na polovični višini vrha, takrat enačbo zapišemo: N = 5.54 ( t r w 1 2 ) 2 kjer je:w 1/2 širina vrha na polovični višini vrha. 14
15 Kromatografski parametri - kapacitivni faktor Razmerje med t' r in t m opisuje termodinamsko povezavo med topljencem v določenem kromatografskem sistemu, pri ravnotežnih pogojih nam to razmerje pove relativno število molekul topljenca v stacionarni oziroma mobilni fazi. Temu razmerju pravimo kapacitivni faktor - k', ki ga izračunamo: k = t r t m Kapacitivni faktor in retencijski čas sta odvisna od dolžine kolone in pretoka mobilne faze. Če je pretok mobilne faze nizek ali če uporabimo daljšo kolono, je daljši retencijski čas in posledično višji kapacitivni faktor. Idealne vrednosti kapacitivnega faktorja so v območju med 1 in 5. Kadar je kapacitivni faktor mnogo manjši od 1, so se spojine eluirale prehitro, če pa je večji od 20, so retencijski časi zelo dolgi oz. predolgi. Kromatografski parametri - selektivnost Selektivnost (α), predstavlja razmerje kapacitivnih faktorjev dveh spojin A in B. α = k B k A = t r B t m t r A t m Spojina A mora imeti vedno krajši retencijski čas od spojine B. V skladu s tem je selektivnost enaka 1, ko se analita med sabo ne ločita, večja od 1 pa je takrat, ko je t rb večji od t ra in sta komponenti ločeni. Selektivnost je odvisna od narave stacionarne faze, sestave mobilne faze in lastnosti analitov. Za izboljšanje selektivnosti spreminjamo oz. menjamo stacionarno fazo ali mobilno fazo ali obe. Kromatografski parametri - ločljivost Ločljivost (R s ) predstavlja sposobnost kromatografske kolone, da loči dva analita. Definirana je kot razmerje med razliko v retencijskih časih dveh vrhov in povprečno širino teh vrhov. Idealno ločljivost na bazni liniji dosežemo takrat, ko so vrednost R s med 1,5 in 2,0. R s = t r2 t r1 w b2 +w b1 2 kjer je: t r retencijski čas komponente, w b širina vrha pri bazni liniji v časovni enoti. 15
16 Kromatografski parametri - ločljivost Kromatografski parametri - simetričnost Pri idealnih pogojih bi morali biti kromatografski vrhovi popolnoma simetrični, njihova oblika pa bi morala biti podobna Gaussovi krivulji. Toda v realnosti mnogo vrhov ni popolnoma simetričnih, pojavlja se lahko ''fronting'' ali ''tailing'' kromatografskega vrha. Asimetrijski faktor (A f ) se uporablja za določanje stopnje simetrije in je definiran pri 10 % višini vrha: Kromatografski parametri - simetričnost A f = b a Faktor simetrije (T f ), ki se uporablja predvsem v farmacevtski industriji, se izračuna nekoliko drugače v tem primeru sta a in b leva in desna širina vrha na 5 % višini vrha. T f = a+b 2a Nepopolno ločena vrhova Popolnoma ločena vrhova R = 1,5 Sprejemljive vrednosti za A f in T f so do 2. Kadar je vrednost T f = 1, to pomeni, da je vrh popolnoma simetričen, če pa je ta vrednost nižja od 1 govorimo o ''frontingu'' kromatografskega vrha. Popolnoma simetričen vrh Nesimetričen vrh 16
17 Prikaz nesimetričnosti kromatografskih vrhov Kromatografski parametri vpliv α in N Van Deemterjeva enačba Klasična teorija podov ne razlaga vpliva: - velikosti delcev, - difuzije, - pretoka, - temperature, - nekaterih drugih dejavnikov na širitev kromatogrfaskih vrhov. A slaba ločljivost, B - večji N boljša ločljivost, (npr. lastnost SF, pretok MF), C enak N, boljša selektivnost, daljši čas analize, (sprememba MF, SF, temperature itd.) D slaba ločljivost, (vpliv L - prekratka kolona na N) Pri kromatografskih določitav sočasno poteka več različnih kinetičnih in termodinamsko kontroliranih procesov: - motnje v pretoku mobilne faze, - difuzija v mobilni fazi, - nepopolno medfazno ravnotežje. Zato zapišemo H kot vsoto: H = H s + H m + H p + H d + H sm kjer je: H s in H m - učinek zaradi prenosa SF in MF, H p - vpliv vrtinčastega toka, H d - vpliv vzdolžne difuzije po koloni in H sm vpliv MF v porah SF. 17
18 Plinska kromatografija Kaj je dekonvolucija kromatografskih vrhov? Plinska kromatografija Odvisnost H vs. u s prikazanimi posameznimi prispevki: H s, H m, H d, H sm eksperimentalne vrednosti Plinska kromatografija Dekonvolucija kromatografskih vrhov s programsko opremo je pristop, ki ga uporabimo samo v primerih, ko kljub optimizaciji kromatografskih pogojev ne uspemo ustrezno ločiti vrhov. 18
19 Van Deemterjeva enačba za GC Van Demterjeva enačba H = A + B/u + u(c s + C m ) Značilni H/u diagrami pri plinski kromatografiji Plinska kromatografija Primerjava H/u diagramov za He, H 2 in N 2 pri GC Plinska kromatografija kjer je A vrtinčast pretok, u hitrost MF, B aksialna difuzija, C s in C m masni prenos na fazni meji. A - Vpliv vrtinčastega pretoka t.i. Eddy diffusion, velikost delcev, polnjenje in geometrija kolone. Manjši delci višji tlaki a bolj enakomerno polnjenje kolone. B/u aksialna difuzija, prispevek je večji pri GC, posebno pri kapilarnih kolonah, medtem ko pri HPLC postane opazen pri zelo nizkih pretokih MF. u(c s + C m ) prenos snovi na fazni meji, vpliv pretoka MF in debeline ter lastnosti SF. Vrednost u linearna hitrost določimo iz zveze u=h/t r, tako, da na kolono dolžine L injiciramo spojino, ki se na koloni ne zadržuje in izmerimo čas njenega potovanja skozi kolono. 19
20 Kromatografija - povzetek 2 ( Ločljivost ali resolucija R W W tr1 tr2) 1 2 k2 Selektivnost k Število teoretskih podov N = L / H (dolžina kolone, H višina poda) Teorija podov je osnova separacije na koloni (NN 1952 Martin, Syrneg), ki pa ne pojasni vpliva velikosti delcev, difuzije, pretoka in temperature na širitve vrhov. Gre za vrsto kinetičnih in termodinamskih parametrov, ki so difuzijsko kontrolirani. Vsi so posledica: motenj v pretoku mobilne faze, difuzije mobilne faze in nepopolnega ravnotežja med fazama. H = H s + H m + H p + H d + H sm Van Demterjeva enačba H = A + B/u + u(c s + C m ) kjer je A vrtinčast pretok, u hitrost MF, B aksialna difuzija, C s in C m masni prenos na fazni meji. 1 Kromatografski trikotnik kromatografske ločbe so vedno kompromis glede ločljivosti, hitrosti in kapacitete množine analiziranega vzorca!!! Kvantitativna kromatografska analiza pristopi Osnova kvantitativne analize je površina kromatografskega vrha. Površino določimo s pomočjo integratorja ali programske opreme in je odvisna od eksperimentalnih pogojev analize, zato vedno primerjamo površine kromatografskih vrhov standardnih raztopin in vzorcev! Odziv detektorja mora biti linearen, posebej pomemben je signal bazne linije, še posebej pri nizkih koncentracijah analitov. Pri sodobni kvantitativni analizi uporabljamo metode: eksternega standarda, večtočkovne kalibracije, metodo standardnega dodatka in metodo internega standarda. 20
21 Kvantitativna kromatografska analiza Pazimo na: linearno območje detektorja, zveznost signala, bazno liniji, definicijo vrha razmerje signal/šum, začetek oz. konec krom. vrha, koelucijo oz. dekonvolucijo vrhov itd... Metoda eksternega standarda C ref. = C s = K A ref. = K A s in C vz. = C x = K A vz. = K A x sledi: C vz. = C ref. A vz. / A ref. oziroma C x = C s A x / A s Metoda internega standarda Interni standard je spojina, ki jo dodamo v vzorec in mora biti: - čist, - inerten, stabilen in - ne sme biti predhodno prisoten v vzorcu. Imeti mora podobne kemijske lastnosti kot analit a ne sme vplivati na samo ločbo. Koncentracijsko območje mora biti ustrezno izbrano prilagojeno, prav tako območje elucije oz. R f. 21
22 Princip nizkotlačne kolonske kromatografije 22
23 Polnjene kolone Vrste kolon POLNJENE KAPILARNE Načini injiciranja Kapilarna kolona ročno z brizgo (siringo) s plinsko brizgo iz plinske faze nad vzorcem (angl. headspace) avtomatski vzorčevalnik desorpcija s pasti ipd. 23
24 Nanašanje vzorca v polnjene kolone Plinska kromatografija GC (GLC, GSC) Plinska kromatografija Uporablja se za ločevanje in določanje hlapnih termično stabilnih spojin merilec tlaka injiciranje vzorca injektor detektor obdelava podatkov Kolone in polnila Polnjena: iz stekla, kovine; polnilo: adsorbenti, silikagel, diatomejske zemlje... (kot nosilci tekoče SF) Kapilarna: (ali: odprta; angl. open tubular, OT): adsorpcijska SF: PLOT (angl. porous layer OT), tekoča SF na nosilcu: SCOT (angl. support-coated OT), tekoča SF na steni: WCOT (angl. wall-coated OT), iz kremenčevega stekla: FSOT (angl. fused-silica OT). kolona Važno še: dolžina, notranji premer, debelina SF. jeklenka z nosilnim plinom termostatirana pečica 24
25 Temperaturno programirana analiza HPLC Kolone Material: nerjaveče jeklo,steklene kolone t / min a) izotermno, nizka T b) izotermno, visoka T c) temperaturno programiranjenevarnosti H = A + B/T + CT Vplivamo na topnost v stacionarni fazi mobilna faza črpalka črpalka mešalec vzorec injektor kolona zapis detektor odpad Izokratska kdaj? Gradientna analiza-za ločevanje več spojin različnih polarnosti Črpalke kontinuirne batne črpalke s kombinacijo ventilov diskontinuirne batne za majhne pretoke Dimenzije: premer: 2-5mm, večji preparativne Stacionarne faze dolžina: 5-25cm polnilo: delci sferični, pod 10 m NP normalno fazna kromatografija Polarna stacionarna faza Mobilna faza nepolarna (ogljikovodiki) 5% RP reverzno fazna kromatografija kromatografija z obrnjeno fazo Nepolarna stacionarna faza Mobilna faza polarna (voda/metanol/acetonitril) 94% 25
26 Izbira topila za raztapljanje vzorca Topilo naj bo enako kot je sestava mobilne faze v začetku analize Polarne vzorce raztopimo v vodi (dodatek metanola/acetonitrila, ph) in analiziramo na nepolarnih (RP) kolonah Popačenje kromatogramov zaradi spremembe mobilne faze! Spektrofotometrični detektorji Standardni UV-VIS, z nizom dinod (volumen celice do 20 L), mikrocelice? Spektrofotometrični detektorji Beerov zakon A= a l c izvedba celice za nizke koncentracije izvedba za preparativno ločevanje Problem: absorpcija svetlobe v mobilni fazi: UV-čista topila Vsa topila in dodatki problematični, če merimo absorbanco pri λ pod 220nm (acetatni pufri!) primerni fosfatni pufri Kvantitativna analiza Priprava umeritvene krivulje (standarne raztopine) ploščina kromatografskega vrha-množina 26
27 Vsebina predavanja KAJ JE IONSKA KROMATOGRAFIJA? doc. dr. Mitja Kolar Osnove in vrste IC kromatografije Vrednotenje kromatogramov Razvoj, merilni sistem in teorija ionske izmenjave pri ionski kromatografiji Uporabnost IC kromatografije s primeri Dodatna literatura Kromatografska separacija je posledica razlik v potovanju posameznih komponent pod vplivom mobilne faze, zaradi selektivnega zadrževanja ali retencije komponent na stacionarni fazi. Ionska kromatografija zajema postopke separacije kemijskih spojin - prevladujoča interakcija je ionska izmenjava. 27
28 Vrste kromatografskih metod Plinska kromatografija (GC) Superkritična tekočinska kromatografija (SFC) Tekočinska kromatografija (LC) Rezultat analize = kromatogram Kolonska Tankoplastna (TLC) Visokotlačna (HPLC) Nizkotlačna (LPLC, MPLC) porazdelitev (LLC) adsorbcija (LSC) izločitev (EC) ionska izmenjava (HP-IC, HP-ICE, MP-IC) 28
29 Kromatogram t R - retencijski čas, je definiran kot čas, zadrževanja merjene komponente analita na koloni. t R je identifikacija za vrsto eluirane zvrsti, a je odvisen od dimenzije kolone, vrste stacionarne in mobilne faze, pretoka, velikosti delcev v koloni in temperature. Kvantitativno merilo za koncentracijo eluirano zvrsti je: površina kromatografskega vrha višina kromatografskega vrha širina kromatografskega vrha na polovični višini. Kromatografija - osnovni pojmi 2 ( Ločljivost ali resolucija R W W tr1 tr2) 1 2 k2 Selektivnost k Število teoretskih podov N = L / H (dolžina kolone, H višina poda) Teorija podov je osnova separacije na koloni (NN 1952 Martin, Syrneg), ki pa ne pojasni vpliva velikosti delcev, difuzije, pretoka in temperature na širitve vrhov. Gre za vrsto kinetičnih in termodinamskih parametrov, ki so difuzijsko kontrolirani. Vsi so posledica: motenj v pretoku mobilne faze, difuzije mobilne faze in nepopolnega ravnotežja med fazama. H = H s + H m + H p + H d + H sm Van Demterjeva enačba H = A + B/u + u(c s + C m ) kjer je A vrtinčast pretok, u hitrost MF, B aksialna difuzija, C s in C m masni prenos na fazni meji. 1 MEDNARODNA OZNAKA ZA IONSKO KROMATOGRAFIJO = IC IONSKA KROMATOGRAFIJA (SLO) ION CHROMATOGRAPHY (ANG) IONENCHROMATOGRAPHIE (D) ION (gr. ion potujoči) naelektren delec KROMATOGRAFIJA (gr. chroma barva; gr. graphein pisati) Danes je IC ločevanje in določevanje koncentracij nabitih zvrsti na trdi stacionarni fazi v koloni, ki poteka pretežno zaradi procesa ionske izmenjave. 29
30 Ionska kromatografija skozi čas I Ionska kromatografija skozi čas II Ionska kromatografija Ruski botanik Mihail Cvet na koloni, polnjeni s CaCO 3 loči rastlinske pigmente klorofile in ksantofile začetek kromatografij (1903). Gline in zeoliti predstavljata večji skupini naravnih ionskih izmenjevalcev. Prvi sintetični ionski izmenjevalci so se sprva uporabljali za mehčanje vode, deionizacijo in čiščenje raztopin (1930). Raziskave v okviru Projekta Manhattan postavijo teoretske osnove ionske izmenjave (1945). Razvoj sodobne tekočinske kromatografije (s teorijo porazdelitvene kromatografije Martin in Synge leta 1952 prejmeta Nobelovo nagrado za kemijo) začetek sodobne IC (Small, Stevens in Baumann) uporabijo ionsko izmenjavo na koloni in detektor za merjenje prevodnosti za določanje anionov in kationov. Hiter razvoj ionske kromatografije do danes ne preseneča saj predstavlja hitro, sočasno, zanesljivo in natančno analitsko metodo. HP-IC (High Performance Ion Chromatography) Ionska izmenjevalna kromatografija visoke ločljivosti Proces na koloni: ionska izmenjava in adsorpcija. Analiza anionov in kationov. HP-ICE (High Performance Ion Chromatography Exlusion) Ionska izključitvena kromatografija visoke ločljivosti Proces na koloni: izključitev, adsorpcija. Analiza šibkih organskih kislin, alkoholov, aminokislin, aldehidov in ogljikovih hidratov. MP-IC (Mobile Phase Ion Chromatography ) Kromatografija ionskih parov Proces na koloni: adsorpcija. Analiza kationskih, anionskih površinsko aktivnih snovi, kovinskih kompleksov in maščobnih kislin. Neodvisno od vrste ionske kromatografije le te delimo na: enokolonsko ali nesupresirano ionsko kromatografijo, dvokolonsko ali supresirano ionsko kromatografijo. 30
31 Enokolonski in dvokolonski sistemi v ionski kromatografiji Ionski kromatograf Enokolonska IC MilliQ H 2 O za regeneracijo Dvokolonska IC Detektor Rezervoar mobilne faze Črpalka Supresorska kolona Predkolona Kolona Injektor 31
32 Mobilne faze S spreminjanjem sestave mobilne faze v IC najbolj učinkovito vplivamo na ločitev komponent in na njihove zadrževalne čase. Mobilne faze glede na vrsto IC Anionska: Na 2 CO 3 /NaHCO 3 Selektivnost pri ionski izmenjavi Ionski radij Naboj hidratiziranega iona Vrsta ionskega izmenjevalca in topila Pri izbiri mobilne faze upoštevamo: združljivost z detektorjem, naravo, topnost in koncentracijo analita, ph, puferno kapaciteto, kompleksacijske vplive, mešanje z organskimi topili. Kationska: HCl, H 2 SO 4, oksalat/citrat HPICE: HCl, heksansulfonska kislina MPIC-A: NH 4 OH, TMAOH MPIC-B: HCl, heksansulfonska kislina Sposobnost vezave monovaletnih kationov (K) na izmenjalna mesta pada od Tl + Ag + Cs + Rb + K + NH 4 + Na + H + Li + in za divalentne katione UO 2 2+ Pb 2+ Sr 2+ Ca 2+ Ni +2+ Cd 2+ Cu 2+ Co 2+ Zn 2+ Mg 2+. Za anione sposobnost vezave na izmenjalna mesta pada od SO 4 2- C 2 O 4 2- I - NO 3 - Br - Cl - HCO 2 - CH 3 CO 2 - OH - F -. 32
33 Črpalke v ionski kromatografiji Vrste črpalk v ionski kromatografiji Injektorji v ionski kromatografiji Hitro doseganje visokih tlakov (do 400 atm) Nepulzirajoče delovanje Pretoki med 0,1 in 10 ml/min Ponovljivost in nadzor pretoka (pod 0,5%) Odpornost proti koroziji Gradientno črpanje Recipročne črpalke (z eno, dvema ali več črpalnimi glavami) Membranske črpalke Črpalke z rezervoarjem in batom Črpalke, ki delujejo s pomočjo plina pod tlakom Ponovljivost injiciranj Vnos različnih volumnov Minimalna kontaminacija med injiciranji Enostavnost, robustnost in avtomatizacija V IC porabljamo injektorje z dozirnimi zankami ali loop injektorje, kjer lahko zanko z analitom napolnimo delno ali v celoti. 33
34 Kaj je ionska izmenjava? Ionski izmenjevalci so snovi, ki so pri stiku z raztopino elektrolita sposobni tega vezati, sočasno pa oddati ekvivalentno množino drugega iona, ki je bil vezan na izmenjalnih mestih. Izmenjava poteka do vzpostavitve ravnotežja, na katerega vpliva vrsta eksperimentalnih parametrov (selektivnost, koncentracija, temperatura, izmenjalna kapaciteta ). Stacionarne faze Razlikujejo se po aktivnih funkcionalnih skupinah, ki so vezane na trdnem polimernem nosilcu (polistiren, polimetakrilat). Za določanje kationov se uporabljata močno kisla sulfonska ( SO 3- H + ) in šibko kisla karboksilna ( COO - H + ) funkcionalna skupina. Za določanje anionov se najpogosteje uporabljata močno alkalna kvarterna ( N(CH 3 ) 3+ OH - ) ali šibko alkalna primarna aminska( NH 3+ OH - ) funkcionalna skupina. Stacionarne faze I sinteza polimernega nosilca Reakcija stirena in divenilbenzena vodi do nastanka stiren-divenilbenzenskega polimera 34
35 Stacionarne faze I - sinteza polimernega nosilca Stacionarne faze II vezava funkcionalnih skupin Teorija separacije na koloni I Pri potovanju anionske zvrsti A x- v mobilni fazi skozi kolono, na kateri so vezane N(CH 3 ) 3+ OH - skupine, pride do ionske izmenjave x(rn(ch 3 ) 3+ )OH - (s) + A x- (aq) (RN(CH 3 ) 3+ ) x A x- (s) + xoh - (aq) Reakcija metakrilne kisline in divenilbenzena, ki vodi do nastanka metakrilat-divenilbenzenovega polimera Reakcijski mehanizem vezave ( SO 3- H + ) funkcionalnih skupin na stiren-divenilbenzenski polimer. Reakcijski mehanizem vezave ( NR 3+ OH - ) funkcionalnih skupin na stiren-divenilbenzenski polimer. Pri potovanju kationske zvrsti K x+ v mobilni fazi skozi kolono, na kateri so vezane RSO 3- H + skupine, pride do ionske izmenjave xrso 3- H + (s) + K x+ (aq) (RSO 3- ) x K x+ (s) + xh + (aq) 35
36 Teorija separacije na koloni II K (RN(CH 3 ) 3+ )A x- (s) OH - (aq) (RN(CH 3 ) 3+ )OH - (s) A x- (aq) Zapisana konstanta ravnotežja (K) nam pove, kako se bo nek anion zadrževal med stacionarno in mobilno fazo. Večje vrednosti K kažejo, da se bo anion bolj zadrževal na stacionarni fazi in bo njegov zadrževalni čas na koloni daljši.. Teorija separacije na koloni III (RN(CH 3 ) 3+ )A x- (s) A x- (aq) K (RN(CH 3 ) 3+ )OH - (s) OH - (aq) Ker je koncentracija OH - (aq) A x- (aq) in (RN(CH 3 ) 3+ )OH - (s) (RN(CH 3 ) 3+ )A x- (s), lahko enačbo zapišemo v obliki (RN(CH 3 ) 3+ )A x- (s) c s K D A x- (aq) c m kjer je K D porazdelitveni koeficient, c s koncentracija analita v stacionarni fazi in c m koncentracija analita v mobilni fazi. Vloga supresorske kolone Mobilno fazo pretvori v nediisocirano obliko. Analit pretvori v popolnoma diisocirano - visokoprevodno obliko. Kontinuirna regeneracija, minimalna disperzija v supresorju, minimalna kontaminacija v supresorju (nizka bazna linija), ph obstojnost, odpornost na organska topila in mehanska odpornost. Vrste supresorjev: kemijski in elektrokemijski. 36
37 Delovanje supresorske kolone in reakcije V raztopini se natrijevi ioni izmenjajo s protoni in tako prevedejo močno prevoden natrijev hidrogenkarbonat v malo disociirano ogljikovo kislino Po izmenjavi natrijevega nitrata (V) iz vzorca nastane dušikova (V) kislina V primeru določanja anionov in uporabe karbonatnega pufra kot eluenta se v supresorski koloni kationi (običajno Na + ) vežejo na ionski izmenjevalec, sprosti se ekvivalentna količina H 3 O + ionov, ki pretvorijo HCO 3 - in CO 3 2- ione v CO 2 in vodo, kar bistveno zniža električno prevodnost eluenta. Obenem pa se protiioni merjenih anionov zamenjajo s H 3 O + ioni in na ta način se bistveno poviša prevodnost merjenega ionskega para (H 3 O + / ustrezni anion). Delovanje elektrokemijskega supresorja Delovanje kemijskega supresorja 37
38 Detektor za merjenje prevodnosti Električna prevodnost je sposobnost elektrolitov, da prevajajo električni tok med dvema paroma koncentričnih Pt elektrod, ki so v električnem polju. Koncentracija - število ionov, njihov naboj, velikost, hitrost in temperatura vplivajo na prevodnost raztopin. Upornost,Ohmov zakon R= U / I [Ω] Prevodnost G = 1 / R [Ω -1, S - Siemens] Specifična upornost ρ (R = ρ l / A) [Ωm, Ωcm] Specifična prevodnost χ = (1 / ρ) [Ω -1 m -1, Ω -1 cm -1 ] Molska prevodnost Λ = χ / c [Sm 2 mol -1 ] Princip merjenja prevodnosti Z višanjem potenciala med elektrodama se veča tudi hitrost ionov v raztopini, zato je odziv detektorja odvisen od uporabljenega potenciala. Uporabljamo oscilirajoče sinusoidne ali pulzirajoče napetosti square, ki znižujejo moteče procese zaradi nastanka kapacitivne dvojne plasti ali Faradayskih elektrolitskih procesov. Uporabljene napetosti imajo ν med 100 in Hz, zgornja meja je 1 MHz. Moteče procese lahko uspešno zmanjšamo tudi z uporabo štiri elektrodne celice za merjenje prevodnosti (med dvema notranjima referenčnima elektrodama je konstanten E, tok teče med zunanjima elektrodama, ko se prevodnost začne spreminjati beležimo tok, ki je potreben za vzdrževanje E in je proporcionalen prevodnosti. Detektor za merjenje prevodnosti + Visoka občutljivost + Univerzalnost za vse nabite analite + Odziv na spremembe koncentracij + Enostaven za izdelavo in miniaturizacijo + Nizka cena in enostavno vzdrževanje - Ni občutljiv za šibko disociirane zvrsti - Odziva se tudi na sestavo mobilne faze 38
39 Drugi detektorji v IC Spektrofotometrija UV/VIS, AES, AAS Spektrometrija z induktivno sklopljeno plazmo ICP-AES Masna spektrometrija z induktivno sklopljeno plazmo ICP-MS Elektrokemijska detekcija (amperometrija, voltametrija, kulometrija in potenciometrija) Uporabimo lahko vsak detektor, ki omogoča pretočno izvedbo! Določanje koncentracij v IC IC je relativna tehnika saj rezultate primerjamo s standardom! Umeritvena krivulja, naj zajema interval pričakovanih koncentracij vzorcev in naj vsebuje najmanj 6 točk. Uvedemo lahko interni standard in uporabimo umeritveno krivuljo kar minimizira merilno napako, vendar idealnega internega standarda pogosto nimamo. Standardni dodatek uporabimo, kadar imamo na voljo malo vzorca. Analizo ponovimo z več standardnimi dodatki različnih koncentracij. Primeri uporabe IC Okolje analiza pitnih, površinskih in industrijskih vod (anioni, kationi, površinsko aktivne snovi) Živilska industrija (pijače, mleko, meso, ribe, sir, konzervirana hrana, olja) Industrija polprevodnikov (topila, kisline, baze) Klinična kemija Kmetijstvo Papirna industrija Gradbeništvo Naftna industrija 39
40 Realni kromatogram, določanje kationov Realni kromatogram, določanje anionov Analiza anionov IC primer Vzorčenje pitne vode 500 ml po ustreznem protokolu, hranjenje, filtracija. Sušenje soli in priprava standardnih raztopin Cl -, NO 3 - SO 4 2- v mill-q vodi (10 mg/l, 20 mg/l, 40 mg/l, 50 mg/l, 60 mg/l) Kalibracija in priprava umeritvenih krivulj za anione Analiza realnih vzorcev Interpretacija rezultatov s komentarji 40
41 Analiza anionov IC primer UK Dodatna literatura in viri Principles of Instrumental Analysis, D.A. Skoog, J.J. Leary. Analytical Chemistry, D.A. Skoog, D.M. West, F.J. Holer. Ion Chromatography A. Huthig. Ion Chromatography, P.R. Haddad, P.E. Jackson. Handbook of Ion Chromatography, J. Weiss
TOPILO IZSTOPNI VENTIL CILINDER KOLONA DUŠILEC
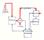 TOPILO VSTOPNI VENTIL CILINDER BAT IZSTOPNI VENTIL KOLONA DUŠILEC HPLC: 1. PORAZDELITVENA ( liquid-liquid ) 2. IONSKA 3. IZKLJUČITVENA oziroma GELSKA 4. ADSORPCIJSKA oziroma LIQUID-SOLID majhni delci (
TOPILO VSTOPNI VENTIL CILINDER BAT IZSTOPNI VENTIL KOLONA DUŠILEC HPLC: 1. PORAZDELITVENA ( liquid-liquid ) 2. IONSKA 3. IZKLJUČITVENA oziroma GELSKA 4. ADSORPCIJSKA oziroma LIQUID-SOLID majhni delci (
TOPLJENEC ASOCIIRA LE V VODNI FAZI
 TOPLJENEC ASOCIIRA LE V VODNI FAZI V primeru asociacij molekul topljenca v vodni ali organski fazi eksperimentalno določeni navidezni porazdelitveni koeficient (P n ) v odvisnosti od koncentracije ni konstanten.
TOPLJENEC ASOCIIRA LE V VODNI FAZI V primeru asociacij molekul topljenca v vodni ali organski fazi eksperimentalno določeni navidezni porazdelitveni koeficient (P n ) v odvisnosti od koncentracije ni konstanten.
UČNI NAČRT PREDMETA / COURSE SYLLABUS Numerical linear algebra. Študijska smer Study field. Samost. delo Individ. work Klinične vaje work
 Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS Numerična linearna algebra Numerical linear algebra Študijski program in stopnja Study programme and level Univerzitetni študijski program Matematika
Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS Numerična linearna algebra Numerical linear algebra Študijski program in stopnja Study programme and level Univerzitetni študijski program Matematika
UČNI NAČRT PREDMETA / COURSE SYLLABUS. Študijska smer Study field. Samost. delo Individ. work Klinične vaje work
 Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS Statistika Statistics Študijski program in stopnja Study programme and level Univerzitetni študijski program Matematika First cycle academic
Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS Statistika Statistics Študijski program in stopnja Study programme and level Univerzitetni študijski program Matematika First cycle academic
Študijska smer Study field. Samost. delo Individ. work Klinične vaje work. Vaje / Tutorial: Slovensko/Slovene
 UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Kvantna mehanika Course title: Quantum mechanics Študijski program in stopnja Study programme and level Univerzitetni študijski program 1.stopnje Fizika First
UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Kvantna mehanika Course title: Quantum mechanics Študijski program in stopnja Study programme and level Univerzitetni študijski program 1.stopnje Fizika First
UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Analiza 1 Course title: Analysis 1. Študijska smer Study field. Samost. delo Individ.
 UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Analiza 1 Course title: Analysis 1 Študijski program in stopnja Study programme and level Univerzitetni študijski program Finančna matematika First cycle
UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Analiza 1 Course title: Analysis 1 Študijski program in stopnja Study programme and level Univerzitetni študijski program Finančna matematika First cycle
UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Predmet: Analiza 3 Course title: Analysis 3. Študijska smer Study field ECTS
 UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Predmet: Analiza 3 Course title: Analysis 3 Študijski program in stopnja Study programme and level Univerzitetni študijski program Matematika
UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Predmet: Analiza 3 Course title: Analysis 3 Študijski program in stopnja Study programme and level Univerzitetni študijski program Matematika
UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Predmet: Optimizacija 1 Course title: Optimization 1. Študijska smer Study field
 UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Predmet: Optimizacija 1 Course title: Optimization 1 Študijski program in stopnja Study programme and level Univerzitetni študijski program Matematika
UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Predmet: Optimizacija 1 Course title: Optimization 1 Študijski program in stopnja Study programme and level Univerzitetni študijski program Matematika
UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Študijska smer Study field ECTS
 Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Numerične metode Numerical methods Študijski program in stopnja Study programme and level Interdisciplinarni univerzitetni
Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Numerične metode Numerical methods Študijski program in stopnja Study programme and level Interdisciplinarni univerzitetni
UČNI NAČRT PREDMETA / COURSE SYLLABUS. Študijska smer Study field
 UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Course title: Teorija umeritvenih polj Gauge field theory Študijski program in stopnja Study programme and level Študijska smer Study field Letnik Academ
UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Course title: Teorija umeritvenih polj Gauge field theory Študijski program in stopnja Study programme and level Študijska smer Study field Letnik Academ
UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Parcialne diferencialne enačbe Partial differential equations. Študijska smer Study field
 Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Parcialne diferencialne enačbe Partial differential equations Študijski program in stopnja Study programme and level Magistrski
Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Parcialne diferencialne enačbe Partial differential equations Študijski program in stopnja Study programme and level Magistrski
UČNI NAČRT PREDMETA / COURSE SYLLABUS. Študijska smer Study field. Samost. delo Individ. work Klinične vaje work
 Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS Teorija grafov Graph theory Študijski program in stopnja Study programme and level Magistrski študijski program Matematika Master's study
Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS Teorija grafov Graph theory Študijski program in stopnja Study programme and level Magistrski študijski program Matematika Master's study
UČNI NAČRT PREDMETA / COURSE SYLLABUS
 UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Predmet: Izbrana poglavja iz diskretne matematike 1 Course title: Topics in discrete mathematics 1 Študijski program in stopnja Study programme
UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Predmet: Izbrana poglavja iz diskretne matematike 1 Course title: Topics in discrete mathematics 1 Študijski program in stopnja Study programme
UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Diferencialne enačbe. Študijska smer Study field ECTS
 Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Diferencialne enačbe Differential equations Študijski program in stopnja Study programme and level Visokošolski strokovni
Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Diferencialne enačbe Differential equations Študijski program in stopnja Study programme and level Visokošolski strokovni
UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Predmet: Algebra 1 Course title: Algebra 1. Študijska smer Study field ECTS
 UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Predmet: Algebra 1 Course title: Algebra 1 Študijski program in stopnja Study programme and level Univerzitetni študijski program Matematika
UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Predmet: Algebra 1 Course title: Algebra 1 Študijski program in stopnja Study programme and level Univerzitetni študijski program Matematika
UČNI NAČRT PREDMETA / COURSE SYLLABUS ELEKTROKEMIJA ELECTROCHEMISTRY. Študijska smer Study Field
 Predmet: Course Title: UČNI NAČRT PREDMETA / COURSE SYLLABUS ELEKTROKEMIJA ELECTROCHEMISTRY Študijski program in stopnja Study Programme and Level Študijska smer Study Field Letnik Academic Year Semester
Predmet: Course Title: UČNI NAČRT PREDMETA / COURSE SYLLABUS ELEKTROKEMIJA ELECTROCHEMISTRY Študijski program in stopnja Study Programme and Level Študijska smer Study Field Letnik Academic Year Semester
Sinteza homologov paracetamola
 Katedra za farmacevtsko kemijo Sinteza homologov paracetamola Vaje iz Farmacevtske kemije 3 1 Sinteza N-(4-hidroksifenil)dekanamida Vaje iz Farmacevtske kemije 3 2 Vprašanja: 1. Zakaj uporabimo zmes voda/dioksan?
Katedra za farmacevtsko kemijo Sinteza homologov paracetamola Vaje iz Farmacevtske kemije 3 1 Sinteza N-(4-hidroksifenil)dekanamida Vaje iz Farmacevtske kemije 3 2 Vprašanja: 1. Zakaj uporabimo zmes voda/dioksan?
UČNI NAČRT PREDMETA / COURSE SYLLABUS. Študijska smer Study field. Samost. delo Individ. work Klinične vaje work
 Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS Optimizacija Optimization Študijski program in stopnja Study programme and level Visokošolski strokovni študijski program Praktična matematika
Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS Optimizacija Optimization Študijski program in stopnja Study programme and level Visokošolski strokovni študijski program Praktična matematika
UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Študijska smer Study field ECTS
 Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Teorija števil Number theory Študijski program in stopnja Study programme and level Magistrski študijski program Matematika
Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Teorija števil Number theory Študijski program in stopnja Study programme and level Magistrski študijski program Matematika
UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Predmet: Statistika 2 Course title: Statistics 2. Študijska smer Study field
 UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Predmet: Statistika 2 Course title: Statistics 2 Študijski program in stopnja Study programme and level Magistrski študijski program Matematika
UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Predmet: Statistika 2 Course title: Statistics 2 Študijski program in stopnja Study programme and level Magistrski študijski program Matematika
Študijska smer Study field. Samost. delo Individ. work Klinične vaje work. Vaje / Tutorial: Slovensko/Slovene
 UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Matematika 2 Course title: Mathematics 2 Študijski program in stopnja Study programme and level Univerzitetni študijski program 1.stopnje Fizika First cycle
UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Matematika 2 Course title: Mathematics 2 Študijski program in stopnja Study programme and level Univerzitetni študijski program 1.stopnje Fizika First cycle
UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2016/17) Diferencialne enačbe. Študijska smer Study field ECTS
 Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2016/17) Diferencialne enačbe Differential equations Študijski program in stopnja Study programme and level Visokošolski strokovni
Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2016/17) Diferencialne enačbe Differential equations Študijski program in stopnja Study programme and level Visokošolski strokovni
kemijsko tehnologijo Kemija UČNI NAČRT PREDMETA / COURSE SYLLABUS ANALIZNA KEMIJA I ANALYTICAL CHEMISTRY I Študijska smer Study Field
 Predmet: Course Title: UČNI NAČRT PREDMETA / COURSE SYLLABUS ANALIZNA KEMIJA I ANALYTICAL CHEMISTRY I Študijski program in stopnja Study Programme and Level Študijska smer Study Field Letnik Academic Year
Predmet: Course Title: UČNI NAČRT PREDMETA / COURSE SYLLABUS ANALIZNA KEMIJA I ANALYTICAL CHEMISTRY I Študijski program in stopnja Study Programme and Level Študijska smer Study Field Letnik Academic Year
UČNI NAČRT PREDMETA / COURSE SYLLABUS. Študijska smer Study field
 UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Course title: Analiza in prognoza vremena Weather analysis and forecasting Študijski program in stopnja Study programme and level Študijska smer Study field
UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Course title: Analiza in prognoza vremena Weather analysis and forecasting Študijski program in stopnja Study programme and level Študijska smer Study field
UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Študijska smer Study field ECTS Vaje / Tutorial: slovenski / Slovene
 Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Linearna algebra Linear algebra Študijski program in stopnja Study programme and level Visokošolski strokovni študijski
Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Linearna algebra Linear algebra Študijski program in stopnja Study programme and level Visokošolski strokovni študijski
ENAČBA STANJA VODE IN VODNE PARE
 ENAČBA STANJA VODE IN VODNE PARE SEMINARSKA NALOGA PRI PREDMETU JEDRSKA TEHNIKA IN ENERGETIKA TAMARA STOJANOV MENTOR: IZRED. PROF. DR. IZTOK TISELJ NOVEMBER 2011 Enačba stanja idealni plin: pv = RT p tlak,
ENAČBA STANJA VODE IN VODNE PARE SEMINARSKA NALOGA PRI PREDMETU JEDRSKA TEHNIKA IN ENERGETIKA TAMARA STOJANOV MENTOR: IZRED. PROF. DR. IZTOK TISELJ NOVEMBER 2011 Enačba stanja idealni plin: pv = RT p tlak,
UČNI NAČRT PREDMETA / COURSE SYLLABUS. Študijska smer Study field. Samost. delo Individ. work Klinične vaje work
 Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS Linearna algebra Linear algebra Študijski program in stopnja Study programme and level Visokošolski strokovni študijski program Praktična matematika
Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS Linearna algebra Linear algebra Študijski program in stopnja Study programme and level Visokošolski strokovni študijski program Praktična matematika
OPTIMIRANJE IZDELOVALNIH PROCESOV
 OPTIMIRANJE IZDELOVALNIH PROCESOV asist. Damir GRGURAŠ, mag. inž. str izr. prof. dr. Davorin KRAMAR damir.grguras@fs.uni-lj.si Namen vaje: Ugotoviti/določiti optimalne parametre pri struženju za dosego
OPTIMIRANJE IZDELOVALNIH PROCESOV asist. Damir GRGURAŠ, mag. inž. str izr. prof. dr. Davorin KRAMAR damir.grguras@fs.uni-lj.si Namen vaje: Ugotoviti/določiti optimalne parametre pri struženju za dosego
UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Numerične metode 1 Course title: Numerical methods 1. Študijska smer Study field
 UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Numerične metode 1 Course title: Numerical methods 1 Študijski program in stopnja Study programme and level Visokošolski strokovni študijski program Praktična
UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Numerične metode 1 Course title: Numerical methods 1 Študijski program in stopnja Study programme and level Visokošolski strokovni študijski program Praktična
Študijska smer Study field. Samost. delo Individ. work Klinične vaje work. Vaje / Tutorial: Slovensko/Slovene
 UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Numerične metode Course title: Numerical methods Študijski program in stopnja Study programme and level Univerzitetni študijski program 1.stopnje Fizika First
UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Numerične metode Course title: Numerical methods Študijski program in stopnja Study programme and level Univerzitetni študijski program 1.stopnje Fizika First
ENERGY AND MASS SPECTROSCOPY OF IONS AND NEUTRALS IN COLD PLASMA
 UDK621.3:(53+54+621 +66), ISSN0352-9045 Informaclje MIDEM 3~(~UU8)4, Ljubljana ENERGY AND MASS SPECTROSCOPY OF IONS AND NEUTRALS IN COLD PLASMA Marijan Macek 1,2* Miha Cekada 2 1 University of Ljubljana,
UDK621.3:(53+54+621 +66), ISSN0352-9045 Informaclje MIDEM 3~(~UU8)4, Ljubljana ENERGY AND MASS SPECTROSCOPY OF IONS AND NEUTRALS IN COLD PLASMA Marijan Macek 1,2* Miha Cekada 2 1 University of Ljubljana,
UČNI NAČRT PREDMETA / COURSE SYLLABUS. Študijska smer Study field
 UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Course title: Fizika kondenzirane snovi Condensed Matter Physics Študijski program in stopnja Study programme and level Študijska smer Study field Letnik
UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Course title: Fizika kondenzirane snovi Condensed Matter Physics Študijski program in stopnja Study programme and level Študijska smer Study field Letnik
UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Študijska smer Study field ECTS
 Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Kompleksna analiza Complex analysis Študijski program in stopnja Study programme and level Magistrski študijski program
Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS (leto / year 2017/18) Kompleksna analiza Complex analysis Študijski program in stopnja Study programme and level Magistrski študijski program
OA07 ANNEX 4: SCOPE OF ACCREDITATION IN CALIBRATION
 OA07 ANNEX 4: SCOPE OF ACCREDITATION IN CALIBRATION Table of contents 1 TECHNICAL FIELDS... 2 2 PRESENTING THE SCOPE OF A CALIBRATION LABOORATORY... 2 3 CONSIDERING CHANGES TO SCOPES... 6 4 CHANGES WITH
OA07 ANNEX 4: SCOPE OF ACCREDITATION IN CALIBRATION Table of contents 1 TECHNICAL FIELDS... 2 2 PRESENTING THE SCOPE OF A CALIBRATION LABOORATORY... 2 3 CONSIDERING CHANGES TO SCOPES... 6 4 CHANGES WITH
ija 3 m Kislost-bazi - čnost Hammettove konstante ska ke acevt Farm Izr. prof. dr Izr. prof. dr. Marko Anderluh. Marko Anderluh 23 oktober.
 acevts ska kem mija 3 Farm Kislost-bazičnost Hammettove konstante Izr. prof. dr. Marko Anderluh 23. oktober 2012 Vpliv kislinsko bazičnih lastnosti Vezava na tarčno mesto farmakodinamsko delovanje Topnost/sproščanje
acevts ska kem mija 3 Farm Kislost-bazičnost Hammettove konstante Izr. prof. dr. Marko Anderluh 23. oktober 2012 Vpliv kislinsko bazičnih lastnosti Vezava na tarčno mesto farmakodinamsko delovanje Topnost/sproščanje
UČNI NAČRT PREDMETA / COURSE SYLLABUS ORGANOKOVINSKA IN SUPRAMOLEKULARNA KEMIJA ORGANOMETALLIC AND SUPRAMOLECULAR CHEMISTRY
 Predmet: Course Title: UČNI NAČRT PREDMETA / COURSE SYLLABUS ORGANOKOVINSKA IN SUPRAMOLEKULARNA KEMIJA ORGANOMETALLIC AND SUPRAMOLECULAR CHEMISTRY Študijski program in stopnja Study Programme and Level
Predmet: Course Title: UČNI NAČRT PREDMETA / COURSE SYLLABUS ORGANOKOVINSKA IN SUPRAMOLEKULARNA KEMIJA ORGANOMETALLIC AND SUPRAMOLECULAR CHEMISTRY Študijski program in stopnja Study Programme and Level
UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO
 UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO DEJAN BRUDAR MAGISTRSKA NALOGA MAGISTRSKI ŠTUDIJ INDUSTRIJSKE FARMACIJE Ljubljana, 2014 DEJAN BRUDAR OPTIMIZACIJA PARAMETROV KROMATOGRAFSKE LOČBE Z UPORABO EKSPERIMENTALNIH
UNIVERZA V LJUBLJANI FAKULTETA ZA FARMACIJO DEJAN BRUDAR MAGISTRSKA NALOGA MAGISTRSKI ŠTUDIJ INDUSTRIJSKE FARMACIJE Ljubljana, 2014 DEJAN BRUDAR OPTIMIZACIJA PARAMETROV KROMATOGRAFSKE LOČBE Z UPORABO EKSPERIMENTALNIH
UČNI NAČRT PREDMETA / COURSE SYLLABUS. Študijska smer Study Field
 Predmet: Course Title: UČNI NAČRT PREDMETA / COURSE SYLLABUS ORGANSKA KEMIJA I ORGANIC CHEMISTRY I Študijski program in stopnja Study Programme and Level Študijska smer Study Field Letnik Academic Year
Predmet: Course Title: UČNI NAČRT PREDMETA / COURSE SYLLABUS ORGANSKA KEMIJA I ORGANIC CHEMISTRY I Študijski program in stopnja Study Programme and Level Študijska smer Study Field Letnik Academic Year
UNIVERSITY OF NOVA GORICA GRADUATE SCHOOL SEPARATION OF SMALL MOLECULES ON MONOLITHIC CHROMATOGRAPHIC MATERIALS MASTER'S THESIS.
 UNIVERSITY F NVA GRICA GRADUATE SCHL SEPARATIN F SMALL MLECULES N MNLITHIC CHRMATGRAPHIC MATERIALS MASTER'S THESIS Janez Jančar Mentor: Prof. dr. Aleš Podgornik Nova Gorica, 2013 Abstract In this work,
UNIVERSITY F NVA GRICA GRADUATE SCHL SEPARATIN F SMALL MLECULES N MNLITHIC CHRMATGRAPHIC MATERIALS MASTER'S THESIS Janez Jančar Mentor: Prof. dr. Aleš Podgornik Nova Gorica, 2013 Abstract In this work,
Sinteza homologov paracetamola
 Katedra za farmacevtsko kemijo Sinteza homologov paracetamola Vaje iz Farmacevtske kemije 3 1 Sinteza N-(4-hidroksifenil)dekanamida Vaje iz Farmacevtske kemije 3 2 Praktična izvedba sinteze 1. 4-aminofenol
Katedra za farmacevtsko kemijo Sinteza homologov paracetamola Vaje iz Farmacevtske kemije 3 1 Sinteza N-(4-hidroksifenil)dekanamida Vaje iz Farmacevtske kemije 3 2 Praktična izvedba sinteze 1. 4-aminofenol
Študijska smer Study field Konstrukcijsko mehanske inženirske znanosti Constructional and Mechanical Engineering Sciences. Vrsta predmeta Course type
 UČNI NAČRT PREDMETA COURSE SYLLABUS Predmet Course title AKUSTIČNA EMISIJA IN HRUP ACOUSTICAL EMISSION AND NOISE Študijski program in stopnja Study programme and level Doktorski študijski program STROJNIŠTVO
UČNI NAČRT PREDMETA COURSE SYLLABUS Predmet Course title AKUSTIČNA EMISIJA IN HRUP ACOUSTICAL EMISSION AND NOISE Študijski program in stopnja Study programme and level Doktorski študijski program STROJNIŠTVO
METODE ZA PREDVIDEVANJE (NAPOVEDOVANJE) VODOTOPNOSTI (topnosti spojin v vodi)
 METODE ZA PREDVIDEVANJE (NAPOVEDOVANJE) VODOTOPNOSTI (topnosti spojin v vodi) Delitev metod (metode temeljijo na): 1. Prispevki posameznih skupin v molekuli k aktivnostnemu koeficientu spojine v vodi.
METODE ZA PREDVIDEVANJE (NAPOVEDOVANJE) VODOTOPNOSTI (topnosti spojin v vodi) Delitev metod (metode temeljijo na): 1. Prispevki posameznih skupin v molekuli k aktivnostnemu koeficientu spojine v vodi.
UČNI NAČRT PREDMETA / COURSE SYLLABUS. Študijska smer Study field
 UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Course title: Fizika laserjev Laser physics Študijski program in stopnja Study programme and level Študijska smer Study field Letnik Academ ic year Semester
UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Course title: Fizika laserjev Laser physics Študijski program in stopnja Study programme and level Študijska smer Study field Letnik Academ ic year Semester
b) Računske naloge (z osnovami): 1. Izračunaj in nariši tiracijsko krivuljo, če k 10,0mL 0,126M HCl dodajaš deleže (glej tabelo) 0,126M NaOH!
 11. Vaja: Kemijsko ravnotežje II a) Naloga: 1. Izmeri ph destilirane in vodovodne vode, ter razloži njegovo vrednost s pomočjo eksperimentov!. Opazuj vpliv temperature na kemijsko ravnotežje!. Določi karbonatno
11. Vaja: Kemijsko ravnotežje II a) Naloga: 1. Izmeri ph destilirane in vodovodne vode, ter razloži njegovo vrednost s pomočjo eksperimentov!. Opazuj vpliv temperature na kemijsko ravnotežje!. Določi karbonatno
Biološka ekvivalenca Statistične metode. Iztok Grabnar
 Biološka ekvivalenca Statistične metode Iztok Grabnar Definicije EMEA: Note for guidance on the investigation of bioavailability and bioequivalence Biološka uporabnost Biovailability means the rate and
Biološka ekvivalenca Statistične metode Iztok Grabnar Definicije EMEA: Note for guidance on the investigation of bioavailability and bioequivalence Biološka uporabnost Biovailability means the rate and
UČNI NAČRT PREDMETA / COURSE SYLLABUS REOLOGIJA KOMPLEKSNIH TEKOČIN. Študijska smer Study Field
 Predmet: Course Title: UČNI NAČRT PREDMETA / COURSE SYLLABUS REOLOGIJA KOMPLEKSNIH TEKOČIN RHEOLOGY OF COMPLEX FLUIDS Študijski program in stopnja Study Programme and Level Študijska smer Study Field Letnik
Predmet: Course Title: UČNI NAČRT PREDMETA / COURSE SYLLABUS REOLOGIJA KOMPLEKSNIH TEKOČIN RHEOLOGY OF COMPLEX FLUIDS Študijski program in stopnja Study Programme and Level Študijska smer Study Field Letnik
Ionska kromatografija. Definicija. Tipi ionske kromatografije 10/24/2013
 Ionska kromatografija Definicija Ionchromatography is a process that allows the separation of ions and polar molecules based on the charge properties of the molecules. Tipi ionske kromatografije Ionska
Ionska kromatografija Definicija Ionchromatography is a process that allows the separation of ions and polar molecules based on the charge properties of the molecules. Tipi ionske kromatografije Ionska
UČNI NAČRT PREDMETA / COURSE SYLLABUS. Študijska smer Study field
 UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Course title: Molekularna biofizika Molceular biophysics Študijski program in stopnja Study programme and level Študijska smer Study field Letnik Academ ic
UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Course title: Molekularna biofizika Molceular biophysics Študijski program in stopnja Study programme and level Študijska smer Study field Letnik Academ ic
CHEM 167 FINAL EXAM MONDAY, MAY 2 9:45 11:45 A.M GILMAN HALL
 PROF. JOHN VERKADE SPRING 2005 THIS EXAM CONSISTS OF 12 QUESTIONS ON 9 PAGES CHEM 167 HOUR EXAM IV APRIL 20, 2005 SEAT NO. NAME RECIT. INSTR. RECIT. SECT. GRADING PAGE Page 2 Page 3 Page 4 Page 5 Page
PROF. JOHN VERKADE SPRING 2005 THIS EXAM CONSISTS OF 12 QUESTIONS ON 9 PAGES CHEM 167 HOUR EXAM IV APRIL 20, 2005 SEAT NO. NAME RECIT. INSTR. RECIT. SECT. GRADING PAGE Page 2 Page 3 Page 4 Page 5 Page
Adsorption of Electrolyte Mixtures in Disordered Porous Media. A Monte Carlo Study
 Acta Chim. Slov. 2007, 54, 503 508 503 Scientific paper Adsorption of Electrolyte Mixtures in Disordered Porous Media. A Monte Carlo Study Gregor Trefalt 1 and Barbara Hribar-Lee 1, * 1 Faculty of Chemistry
Acta Chim. Slov. 2007, 54, 503 508 503 Scientific paper Adsorption of Electrolyte Mixtures in Disordered Porous Media. A Monte Carlo Study Gregor Trefalt 1 and Barbara Hribar-Lee 1, * 1 Faculty of Chemistry
Chromatographic Methods of Analysis Section - 4 : Ion Exchange Chrom. Prof. Tarek A. Fayed
 Chromatographic Methods of Analysis Section - 4 : Ion Exchange Chrom. Prof. Tarek A. Fayed Ion Exchange Chromatography (IEC) In this type of chromatography, the solid stationary phase )organic resin) is
Chromatographic Methods of Analysis Section - 4 : Ion Exchange Chrom. Prof. Tarek A. Fayed Ion Exchange Chromatography (IEC) In this type of chromatography, the solid stationary phase )organic resin) is
Accurately Determining Hydrogen Carbonate in Water in the Presence of or Simultaneously with the Anions of Carboxylic Acids
 210 Acta Chim. Slov. 2007, 54, 210 215 Technical paper Accurately Determining Hydrogen Carbonate in Water in the Presence of or Simultaneously with the Anions of Carboxylic Acids Nata{a Gros,* Andrej Nemarnik
210 Acta Chim. Slov. 2007, 54, 210 215 Technical paper Accurately Determining Hydrogen Carbonate in Water in the Presence of or Simultaneously with the Anions of Carboxylic Acids Nata{a Gros,* Andrej Nemarnik
Last 4 Digits of USC ID:
 Chemistry 05 B Practice Exam Dr. Jessica Parr First Letter of last Name PLEASE PRINT YOUR NAME IN BLOCK LETTERS Name: Last 4 Digits of USC ID: Lab TA s Name: Question Points Score Grader 8 2 4 3 9 4 0
Chemistry 05 B Practice Exam Dr. Jessica Parr First Letter of last Name PLEASE PRINT YOUR NAME IN BLOCK LETTERS Name: Last 4 Digits of USC ID: Lab TA s Name: Question Points Score Grader 8 2 4 3 9 4 0
ICP-MS: Masna spektrometrija z induktivno sklopljeno plazmo
 ICP-MS: Masna spektrometrija z induktivno sklopljeno plazmo ICP-MS vsebina predstavitve Osnove instrumentalne tehnike (princip delovanja, spektralne interference, kvantifikacija) Določitev celotnih koncentracij
ICP-MS: Masna spektrometrija z induktivno sklopljeno plazmo ICP-MS vsebina predstavitve Osnove instrumentalne tehnike (princip delovanja, spektralne interference, kvantifikacija) Določitev celotnih koncentracij
Attempt to prepare seasonal weather outlook for Slovenia
 Attempt to prepare seasonal weather outlook for Slovenia Main available sources (ECMWF, EUROSIP, IRI, CPC.NCEP.NOAA,..) Two parameters (T and RR anomally) Textual information ( Met Office like ) Issued
Attempt to prepare seasonal weather outlook for Slovenia Main available sources (ECMWF, EUROSIP, IRI, CPC.NCEP.NOAA,..) Two parameters (T and RR anomally) Textual information ( Met Office like ) Issued
Odgovor rastlin na povečane koncentracije CO 2. Ekofiziologija in mineralna prehrana rastlin
 Odgovor rastlin na povečane koncentracije CO 2 Ekofiziologija in mineralna prehrana rastlin Spremembe koncentracije CO 2 v atmosferi merilna postaja Mauna Loa, Hawaii. koncentracija CO 2 [μmol mol -1 ]
Odgovor rastlin na povečane koncentracije CO 2 Ekofiziologija in mineralna prehrana rastlin Spremembe koncentracije CO 2 v atmosferi merilna postaja Mauna Loa, Hawaii. koncentracija CO 2 [μmol mol -1 ]
Stopnja protolize(disociacije) - merilo za jakost elektrolita. = c d /c
 Stopnja protolize(disociacije) - merilo za jakost elektrolita = N/N 0 = n/n 0 = c d /c = stopnja protolize (disociacije) N = število disociiranih molekul (HCl) oz. formulskih enot (NaCl) N 0 = število
Stopnja protolize(disociacije) - merilo za jakost elektrolita = N/N 0 = n/n 0 = c d /c = stopnja protolize (disociacije) N = število disociiranih molekul (HCl) oz. formulskih enot (NaCl) N 0 = število
UČNI NAČRT PREDMETA / COURSE SYLLABUS Analiza varnosti in tveganja v medicinski fiziki Evaluation of safety and risk in medical physics
 Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS Analiza varnosti in tveganja v medicinski fiziki Evaluation of safety and risk in medical physics Študijski program in stopnja Study programme
Predmet: Course title: UČNI NAČRT PREDMETA / COURSE SYLLABUS Analiza varnosti in tveganja v medicinski fiziki Evaluation of safety and risk in medical physics Študijski program in stopnja Study programme
Circle the letters only. NO ANSWERS in the Columns! (3 points each)
 Chemistry 1304.001 Name (please print) Exam 4 (100 points) April 12, 2017 On my honor, I have neither given nor received unauthorized aid on this exam. Signed Date Circle the letters only. NO ANSWERS in
Chemistry 1304.001 Name (please print) Exam 4 (100 points) April 12, 2017 On my honor, I have neither given nor received unauthorized aid on this exam. Signed Date Circle the letters only. NO ANSWERS in
Metallurgical Chemistry. An Audio Course for Students
 Laval University From the SelectedWorks of Fathi Habashi February, 1987 Metallurgical Chemistry. An Audio Course for Students Fathi Habashi Available at: https://works.bepress.com/fathi_habashi/27/ METALLURGICAL
Laval University From the SelectedWorks of Fathi Habashi February, 1987 Metallurgical Chemistry. An Audio Course for Students Fathi Habashi Available at: https://works.bepress.com/fathi_habashi/27/ METALLURGICAL
Priloga E.2.2. Uč ni nač rti predmetov v š tudijškem programu EKOLOGIJA IN BIODIVERZITETA
 Priloga E.2.2. Uč ni nač rti predmetov v š tudijškem programu EKOLOGIJA IN BIODIVERZITETA EKOLOGIJA ŽIVALI... 2 EKOSISTEMI... 6 BIOLOGIJA PODZEMNIH HABITATOV... 11 VEDENJE ŽIVALI IN OKOLJE... 15 EKOLOGIJA
Priloga E.2.2. Uč ni nač rti predmetov v š tudijškem programu EKOLOGIJA IN BIODIVERZITETA EKOLOGIJA ŽIVALI... 2 EKOSISTEMI... 6 BIOLOGIJA PODZEMNIH HABITATOV... 11 VEDENJE ŽIVALI IN OKOLJE... 15 EKOLOGIJA
Stehiometrija za študente veterine
 Univerza v Ljubljani Veterinarska fakulteta Stehiometrija za študente veterine Učbenik s praktičnimi primeri za predmet Biokemija Nova, dopolnjena izdaja Petra Zrimšek Ljubljana, 016 Petra Zrimšek Stehiometrija
Univerza v Ljubljani Veterinarska fakulteta Stehiometrija za študente veterine Učbenik s praktičnimi primeri za predmet Biokemija Nova, dopolnjena izdaja Petra Zrimšek Ljubljana, 016 Petra Zrimšek Stehiometrija
Univerzitetni študijski program prve stopnje GEODEZIJA IN GEOINFORMATIKA (BA)
 University of Ljubljana Faculty of Civil and Geodetic Engineering Učni načrti Univerzitetni študijski program prve stopnje GEODEZIJA IN GEOINFORMATIKA (BA) Course syllabi 1 st cycle academic study GEODESY
University of Ljubljana Faculty of Civil and Geodetic Engineering Učni načrti Univerzitetni študijski program prve stopnje GEODEZIJA IN GEOINFORMATIKA (BA) Course syllabi 1 st cycle academic study GEODESY
8. Relax and do well.
 CHEM 1515 Exam II John II. Gelder October 14, 1993 Name TA's Name Lab Section INSTRUCTIONS: 1. This examination consists of a total of 8 different pages. The last two pages include a periodic table, a
CHEM 1515 Exam II John II. Gelder October 14, 1993 Name TA's Name Lab Section INSTRUCTIONS: 1. This examination consists of a total of 8 different pages. The last two pages include a periodic table, a
Secondary Support Pack. be introduced to some of the different elements within the periodic table;
 Secondary Support Pack INTRODUCTION The periodic table of the elements is central to chemistry as we know it today and the study of it is a key part of every student s chemical education. By playing the
Secondary Support Pack INTRODUCTION The periodic table of the elements is central to chemistry as we know it today and the study of it is a key part of every student s chemical education. By playing the
1) V diagramu sta prikazana plazemska koncentracijska profila po večkratnem intravenskem odmerjanju učinkovine v dveh različnih primerih (1 in 2).
 NALOGE ) V diagramu sta prikazana plazemska koncentracijska profila po večkratnem intravenskem odmerjanju učinkovine v dveh različnih primerih ( in ). 0.8 0.6 0.4 0. 0.0 0.08 0.06 0.04 0.0 0.00 0 0 0 30
NALOGE ) V diagramu sta prikazana plazemska koncentracijska profila po večkratnem intravenskem odmerjanju učinkovine v dveh različnih primerih ( in ). 0.8 0.6 0.4 0. 0.0 0.08 0.06 0.04 0.0 0.00 0 0 0 30
CLASS TEST GRADE 11. PHYSICAL SCIENCES: CHEMISTRY Test 4: Matter and materials 1
 CLASS TEST GRADE PHYSICAL SCIENCES: CHEMISTRY Test 4: Matter and materials MARKS: 45 TIME: hour INSTRUCTIONS AND INFORMATION. Answer ALL the questions. 2. You may use non-programmable calculators. 3. You
CLASS TEST GRADE PHYSICAL SCIENCES: CHEMISTRY Test 4: Matter and materials MARKS: 45 TIME: hour INSTRUCTIONS AND INFORMATION. Answer ALL the questions. 2. You may use non-programmable calculators. 3. You
Chemistry 2 Exam Roane State Academic Festival. Name (print neatly) School
 Name (print neatly) School There are fifteen question on this exam. Each question is weighted equally. n the answer sheet, write your name in the space provided and your answers in the blanks provided.
Name (print neatly) School There are fifteen question on this exam. Each question is weighted equally. n the answer sheet, write your name in the space provided and your answers in the blanks provided.
Faculty of Natural and Agricultural Sciences Chemistry Department. Semester Test 1 MEMO. Analytical Chemistry CMY 283
 Faculty of Natural and Agricultural Sciences Chemistry Department Semester Test 1 MEMO Analytical Chemistry CMY 283 Date: 5 September 2016 Lecturers : Prof P Forbes, Dr Laurens, Mr SA Nsibande Time: 90
Faculty of Natural and Agricultural Sciences Chemistry Department Semester Test 1 MEMO Analytical Chemistry CMY 283 Date: 5 September 2016 Lecturers : Prof P Forbes, Dr Laurens, Mr SA Nsibande Time: 90
Magistrski študijski program druge stopnje GEODEZIJA IN GEOINFORMATIKA (MA)
 University of Ljubljana Faculty of Civil and Geodetic Engineering Učni načrti Magistrski študijski program druge stopnje GEODEZIJA IN GEOINFORMATIKA (MA) Course syllabi 2 nd cycle master study GEODESY
University of Ljubljana Faculty of Civil and Geodetic Engineering Učni načrti Magistrski študijski program druge stopnje GEODEZIJA IN GEOINFORMATIKA (MA) Course syllabi 2 nd cycle master study GEODESY
UČNI NAČRT PREDMETA / COURSE SYLLABUS INSTRUMENTALNE METODE INSTRUMENTAL METHODS. Študijska smer Study Field
 Predmet: Course Title: UČNI NAČRT PREDMETA / COURSE SYLLABUS INSTRUMENTALNE METODE INSTRUMENTAL METHODS Študijski program in stopnja Study Programme and Level Študijska smer Study Field Letnik Academic
Predmet: Course Title: UČNI NAČRT PREDMETA / COURSE SYLLABUS INSTRUMENTALNE METODE INSTRUMENTAL METHODS Študijski program in stopnja Study Programme and Level Študijska smer Study Field Letnik Academic
Faculty of Natural and Agricultural Sciences Chemistry Department. Semester Test 1. Analytical Chemistry CMY 283. Time: 120 min Marks: 100 Pages: 6
 Faculty of Natural and Agricultural Sciences Chemistry Department Semester Test 1 Analytical Chemistry CMY 283 Date: 5 September 2016 Lecturers : Prof P Forbes, Dr Laurens, Mr SA Nsibande Time: 120 min
Faculty of Natural and Agricultural Sciences Chemistry Department Semester Test 1 Analytical Chemistry CMY 283 Date: 5 September 2016 Lecturers : Prof P Forbes, Dr Laurens, Mr SA Nsibande Time: 120 min
M10/4/CHEMI/SPM/ENG/TZ2/XX+ CHEMISTRY. Wednesday 12 May 2010 (afternoon) 45 minutes INSTRUCTIONS TO CANDIDATES
 M10/4/CHEMI/SPM/ENG/TZ/XX+ 106116 CHEMISTRY standard level Paper 1 Wednesday 1 May 010 (afternoon) 45 minutes INSTRUCTIONS TO CANDIDATES Do not open this examination paper until instructed to do so. Answer
M10/4/CHEMI/SPM/ENG/TZ/XX+ 106116 CHEMISTRY standard level Paper 1 Wednesday 1 May 010 (afternoon) 45 minutes INSTRUCTIONS TO CANDIDATES Do not open this examination paper until instructed to do so. Answer
CHEM 108 (Spring-2008) Exam. 3 (105 pts)
 CHEM 08 (Spring-008) Exam. (05 pts) Name: --------------------------------------------------------------------------, CLID # -------------------------------- LAST NAME, First (Circle the alphabet segment
CHEM 08 (Spring-008) Exam. (05 pts) Name: --------------------------------------------------------------------------, CLID # -------------------------------- LAST NAME, First (Circle the alphabet segment
(C) Pavel Sedach and Prep101 1
 (C) Pavel Sedach and Prep101 1 (C) Pavel Sedach and Prep101 1 (C) Pavel Sedach and Prep101 2 (C) Pavel Sedach and Prep101 2 (C) Pavel Sedach and Prep101 3 (C) Pavel Sedach and Prep101 3 (C) Pavel Sedach
(C) Pavel Sedach and Prep101 1 (C) Pavel Sedach and Prep101 1 (C) Pavel Sedach and Prep101 2 (C) Pavel Sedach and Prep101 2 (C) Pavel Sedach and Prep101 3 (C) Pavel Sedach and Prep101 3 (C) Pavel Sedach
oblika število ur število KT izvaja Predavanja 45 1,5 učitelj Seminar 30 1 učitelj, sodelavec SKUPAJ 75 2,5
 UČNI NAČRT: Analiza IV Realna analiza Osnovni podatki o predmetu 1. Ime predmeta: Analiza IV Realna analiza 2. Število KT (seštevek iz tabel spodaj): 6 3. Učni jezik: slovenski Podatki o umeščenosti predmeta
UČNI NAČRT: Analiza IV Realna analiza Osnovni podatki o predmetu 1. Ime predmeta: Analiza IV Realna analiza 2. Število KT (seštevek iz tabel spodaj): 6 3. Učni jezik: slovenski Podatki o umeščenosti predmeta
8. Relax and do well.
 CHEM 1225 Exam I John I. Gelder February 4, 1999 Name KEY TA's Name Lab Section Please sign your name below to give permission to post your course scores on homework, laboratories and exams. If you do
CHEM 1225 Exam I John I. Gelder February 4, 1999 Name KEY TA's Name Lab Section Please sign your name below to give permission to post your course scores on homework, laboratories and exams. If you do
Solutions and Ions. Pure Substances
 Class #4 Solutions and Ions CHEM 107 L.S. Brown Texas A&M University Pure Substances Pure substance: described completely by a single chemical formula Fixed composition 1 Mixtures Combination of 2 or more
Class #4 Solutions and Ions CHEM 107 L.S. Brown Texas A&M University Pure Substances Pure substance: described completely by a single chemical formula Fixed composition 1 Mixtures Combination of 2 or more
Transport snovi preko celičnih membran. Lodish et al. 4. izdaja, 15. poglavje (str )
 Transport snovi preko celičnih membran Lodish et al. 4. izdaja, 15. poglavje (str. 578 615) Relativna propustnost fosfolipidnega dvosloja za različne molekule Načini transporta snovi preko celičnih membran
Transport snovi preko celičnih membran Lodish et al. 4. izdaja, 15. poglavje (str. 578 615) Relativna propustnost fosfolipidnega dvosloja za različne molekule Načini transporta snovi preko celičnih membran
INSTRUCTIONS: Exam III. November 10, 1999 Lab Section
 CHEM 1215 Exam III John III. Gelder November 10, 1999 Name TA's Name Lab Section INSTRUCTIONS: 1. This examination consists of a total of 7 different pages. The last page includes a periodic table and
CHEM 1215 Exam III John III. Gelder November 10, 1999 Name TA's Name Lab Section INSTRUCTIONS: 1. This examination consists of a total of 7 different pages. The last page includes a periodic table and
Študijska smer Study field. Klinične vaje work. Nosilec predmeta / prof. dr. Peter Legiša, prof. dr. Bojan Magajna, prof. dr.
 UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Matematika 1 Course title: Mathematics 1 Študijski program in stopnja Study programme and level Univerzitetni študijski program 1.stopnje Fizika First cycle
UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Matematika 1 Course title: Mathematics 1 Študijski program in stopnja Study programme and level Univerzitetni študijski program 1.stopnje Fizika First cycle
Chemistry Standard level Paper 1
 Chemistry Standard level Paper 1 Thursday 12 May 2016 (morning) 45 minutes Instructions to candidates Do not open this examination paper until instructed to do so. Answer all the questions. For each question,
Chemistry Standard level Paper 1 Thursday 12 May 2016 (morning) 45 minutes Instructions to candidates Do not open this examination paper until instructed to do so. Answer all the questions. For each question,
Analizna kemija II in industrijska analiza
 Univerza v Mariboru Fakulteta za kemijo in kemijsko tehnologijo Maša Islamčević Razboršek in Mitja Kolar Analizna kemija II in industrijska analiza Navodila za vaje Maribor, januar 2016 Maša Islamčević
Univerza v Mariboru Fakulteta za kemijo in kemijsko tehnologijo Maša Islamčević Razboršek in Mitja Kolar Analizna kemija II in industrijska analiza Navodila za vaje Maribor, januar 2016 Maša Islamčević
8. Relax and do well.
 CHEM 1225 Exam III John III. Gelder April 8, 1999 Name TA's Name Lab Section INSTRUCTIONS: 1. This examination consists of a total of 7 different pages. The last two pages includes a periodic table and
CHEM 1225 Exam III John III. Gelder April 8, 1999 Name TA's Name Lab Section INSTRUCTIONS: 1. This examination consists of a total of 7 different pages. The last two pages includes a periodic table and
Chapter 3: Stoichiometry
 Chapter 3: Stoichiometry Chem 6A Michael J. Sailor, UC San Diego 1 Announcements: Thursday (Sep 29) quiz: Bring student ID or we cannot accept your quiz! No notes, no calculators Covers chapters 1 and
Chapter 3: Stoichiometry Chem 6A Michael J. Sailor, UC San Diego 1 Announcements: Thursday (Sep 29) quiz: Bring student ID or we cannot accept your quiz! No notes, no calculators Covers chapters 1 and
30 Zn(s) 45 Rh. Pd(s) Ag(s) Cd(s) In(s) Sn(s) white. 77 Ir. Pt(s) Au. Hg(l) Tl. 109 Mt. 111 Uuu. 112 Uub. 110 Uun. 65 Tb. 62 Sm. 64 Gd. 63 Eu.
 Enthalpy changes: experimentally it is much easier to measure heat flow at const pressure - this is enthalpy q p = )H : also nearly all chemical reactions are done at constant pressure. Enthalpy (heat)
Enthalpy changes: experimentally it is much easier to measure heat flow at const pressure - this is enthalpy q p = )H : also nearly all chemical reactions are done at constant pressure. Enthalpy (heat)
M09/4/CHEMI/SPM/ENG/TZ1/XX+ CHEMISTRY. Monday 18 May 2009 (afternoon) 45 minutes INSTRUCTIONS TO CANDIDATES
 M09/4/CHEMI/SPM/ENG/TZ1/XX+ 22096110 CHEMISTRY standard level Paper 1 Monday 18 May 2009 (afternoon) 45 minutes INSTRUCTIONS TO CANDIDATES Do not open this examination paper until instructed to do so.
M09/4/CHEMI/SPM/ENG/TZ1/XX+ 22096110 CHEMISTRY standard level Paper 1 Monday 18 May 2009 (afternoon) 45 minutes INSTRUCTIONS TO CANDIDATES Do not open this examination paper until instructed to do so.
TRU Chemistry Contest Chemistry 12 May 21, 2003 Time: 90 minutes
 TRU Chemistry Contest Chemistry 12 May 21, 2003 Time: 90 minutes Last Name First name School Teacher Please follow the instructions below. We will send your teacher a report on your performance. Top performers
TRU Chemistry Contest Chemistry 12 May 21, 2003 Time: 90 minutes Last Name First name School Teacher Please follow the instructions below. We will send your teacher a report on your performance. Top performers
7. Relax and do well.
 CHEM 1215 Exam II John II. Gelder October 7, 1998 Name TA's Name Lab Section INSTRUCTIONS: 1. This examination consists of a total of 5 different pages. The last page includes a periodic table and a solubility
CHEM 1215 Exam II John II. Gelder October 7, 1998 Name TA's Name Lab Section INSTRUCTIONS: 1. This examination consists of a total of 5 different pages. The last page includes a periodic table and a solubility
UNIVERZA V MARIBORU FAKULTETA ZA KEMIJO IN KEMIJSKO TEHNOLOGIJO. Simonič Marjana TEHNOLOGIJA VOD. Laboratorijske vaje
 UNIVERZA V MARIBORU FAKULTETA ZA KEMIJO IN KEMIJSKO TEHNOLOGIJO Simonič Marjana TEHNOLOGIJA VOD Laboratorijske vaje Maribor, Februar 2004 DOLOČITEV OBARVANOSTI IN MOTNOSTI 1. Namen Določimo obarvanost
UNIVERZA V MARIBORU FAKULTETA ZA KEMIJO IN KEMIJSKO TEHNOLOGIJO Simonič Marjana TEHNOLOGIJA VOD Laboratorijske vaje Maribor, Februar 2004 DOLOČITEV OBARVANOSTI IN MOTNOSTI 1. Namen Določimo obarvanost
Multipla korelacija in regresija. Multipla regresija, multipla korelacija, statistično zaključevanje o multiplem R
 Multipla koelacia in egesia Multipla egesia, multipla koelacia, statistično zaklučevane o multiplem Multipla egesia osnovni model in ačunane paametov Z multiplo egesio napoveduemo vednost kiteia (odvisne
Multipla koelacia in egesia Multipla egesia, multipla koelacia, statistično zaklučevane o multiplem Multipla egesia osnovni model in ačunane paametov Z multiplo egesio napoveduemo vednost kiteia (odvisne
Študijska smer Study field. Samost. delo Individ. work Klinične vaje work. Vaje / Tutorial: Slovensko/Slovene
 UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Matematika III Course title: Mathematics III Študijski program in stopnja Study programme and level Univerzitetni študijski program 1.stopnje Fizika First
UČNI NAČRT PREDMETA / COURSE SYLLABUS Predmet: Matematika III Course title: Mathematics III Študijski program in stopnja Study programme and level Univerzitetni študijski program 1.stopnje Fizika First
If anything confuses you or is not clear, raise your hand and ask!
 CHM 1045 Dr. Light s Section December 10, 2002 FINAL EXAM Name (please print) Recitation Section Meeting Time This exam consists of six pages. Make sure you have one of each. Print your name at the top
CHM 1045 Dr. Light s Section December 10, 2002 FINAL EXAM Name (please print) Recitation Section Meeting Time This exam consists of six pages. Make sure you have one of each. Print your name at the top
ENERGY AND MASS DISTRIBUTIONS OF IONS DURING DEPOSTITION OF TiN BY TRIODE ION PLATING IN BAI 730 M
 ISSN 1318-0010 KZLTET 32(6)561(1998) M. MA^EK ET AL.: ENERGY AND MASS DISTRIBUTION OF IONS... ENERGY AND MASS DISTRIBUTIONS OF IONS DURING DEPOSTITION OF TiN BY TRIODE ION PLATING IN BAI 730 M ENERGIJSKE
ISSN 1318-0010 KZLTET 32(6)561(1998) M. MA^EK ET AL.: ENERGY AND MASS DISTRIBUTION OF IONS... ENERGY AND MASS DISTRIBUTIONS OF IONS DURING DEPOSTITION OF TiN BY TRIODE ION PLATING IN BAI 730 M ENERGIJSKE
Lab Day and Time: Instructions. 1. Do not open the exam until you are told to start.
 Name: Lab Day and Time: Instructions 1. Do not open the exam until you are told to start. 2. This exam is closed note and closed book. You are not allowed to use any outside material while taking this
Name: Lab Day and Time: Instructions 1. Do not open the exam until you are told to start. 2. This exam is closed note and closed book. You are not allowed to use any outside material while taking this
Reševanje problemov in algoritmi
 Reševanje problemov in algoritmi Vhod Algoritem Izhod Kaj bomo spoznali Zgodovina algoritmov. Primeri algoritmov. Algoritmi in programi. Kaj je algoritem? Algoritem je postopek, kako korak za korakom rešimo
Reševanje problemov in algoritmi Vhod Algoritem Izhod Kaj bomo spoznali Zgodovina algoritmov. Primeri algoritmov. Algoritmi in programi. Kaj je algoritem? Algoritem je postopek, kako korak za korakom rešimo
Chemistry 185 Exam #2 - A November 5, Lab Day and Time: Instructions. 1. Do not open the exam until you are told to start.
 Name: Lab Day and Time: Instructions 1. Do not open the exam until you are told to start. 2. This exam is closed note and closed book. You are not allowed to use any outside material while taking this
Name: Lab Day and Time: Instructions 1. Do not open the exam until you are told to start. 2. This exam is closed note and closed book. You are not allowed to use any outside material while taking this
The Periodic Table. Periodic Properties. Can you explain this graph? Valence Electrons. Valence Electrons. Paramagnetism
 Periodic Properties Atomic & Ionic Radius Energy Electron Affinity We want to understand the variations in these properties in terms of electron configurations. The Periodic Table Elements in a column
Periodic Properties Atomic & Ionic Radius Energy Electron Affinity We want to understand the variations in these properties in terms of electron configurations. The Periodic Table Elements in a column
8. Relax and do well.
 CHEM 15 Exam II John II. Gelder March 4, 1999 Name TA's Name Lab Section INSTRUCTIONS: 1. This examination consists of a total of 7 different pages. The last two pages includes a periodic table, a solubility
CHEM 15 Exam II John II. Gelder March 4, 1999 Name TA's Name Lab Section INSTRUCTIONS: 1. This examination consists of a total of 7 different pages. The last two pages includes a periodic table, a solubility
Učni načrti Univerzitetni študijski program prve stopnje GEODEZIJA IN GEOINFORMATIKA (BA)
 Univerza v Ljubljani Fakulteta za gradbeništvo in geodezijo Učni načrti Univerzitetni študijski program prve stopnje GEODEZIJA IN GEOINFORMATIKA (BA) Course Syllabi 1 nd cycle academic study GEODESY AND
Univerza v Ljubljani Fakulteta za gradbeništvo in geodezijo Učni načrti Univerzitetni študijski program prve stopnje GEODEZIJA IN GEOINFORMATIKA (BA) Course Syllabi 1 nd cycle academic study GEODESY AND
