PRISTUP SINTEZI 4-NITROZOAZOBENZENA
|
|
|
- Brenda Allison
- 5 years ago
- Views:
Transcription
1 MARIJA SOKOLOVIĆ PRISTUP SINTEZI 4-NITROZOAZOBENZENA Diplomski rad predložen Kemijskom odsjeku Prirodoslovno-matematičkog fakulteta Sveučilišta u Zagrebu radi stjecanja zvanja magistra kemije Zagreb, 2016.
2 Ovaj rad izrađen je na Zavodu za organsku kemiju Kemijskog odsjeka Prirodoslovno-matematičkog fakulteta Sveučilišta u Zagrebu pod mentorstvom prof. dr. sc. Hrvoja Vančika i neposrednim vodstvom dr. sc. Igora Rončevića.
3 Zahvaljujem, mentoru prof. dr. sc. Hrvoju Vančiku na stručnom vodstvu i velikoj ljudskosti koju je pokazao prilikom izrade ovog Diplomskog rada. Profesore, hvala Vam na svemu, prije svega na razumijevanju, pristupačnosti kad god je to trebalo, te ugodnoj atmosferi prilikom izrade Diplomskog rada. Svojim znanjem i ljudskosti pokazali ste da ste veliki čovjek. Zauvijek ćete mi ostati u lijepom sjećanju! Također se zahvaljujem neposrednom voditelju dr. sc. Igoru Rončeviću na svoj nesebičnoj pomoći, svom uloženom trudu i znanju prilikom izrade ovog Diplomskog rada. Hvala Ivanu Nemetu na svoj pomoći tijekom studija, prijateljskom odnosu i podršci. Zahvaljujem se prijateljima i kolegama koji su bili uz mene cijelo vrijeme, a najviše tebi Mateja. Takvu prijateljicu svatko može poželjeti. Posebno hvala majci Ani, bratu Damiru što su bili uvijek uz mene i vjerovali u mene, ali najveće i posebno HVALA baki Mariji.,,Hvala ti bako na svemu što si me naučila od malih nogu, od tablice množenja do pisanja sastavaka, svoj pruženoj ljubavi i veselju, te onome najvažnijem, da sam zahvaljujući tebi postala savjesna, marljiva i poštena osoba. Volim te kao što ti svaki put kažem, najviše na svijetu!
4 SADRŽAJ SAŽETAK... VI ABSTRACT...VII 1. UVOD LITERATURNI PREGLED SVOJSTVA NITROZO SPOJEVA Aromatski nitrozo spojevi Alifatski nitrozo spojevi Priprava nitrozo spojeva AZO SPOJEVI Aminoazobenzeni SPEKTROSKOPSKE METODE U PROUČAVANJU NITROZO I AZO SPOJEVA IR spektroskopija UV/VIS spektroskopija H i 13 C NMR spektroskopija FOTOKROMIZAM I TERMOKROMIZAM NITROZO I AZO-SPOJEVA Fotokromizam i termokromizam nitrozo spojeva u čvrstom stanju EKSPERIMENTALNI DIO MATERIJALI POKUŠAJI PRIPRAVE NITROZOAZOBENZENA Priprava 4-nitronitrozobenzena Priprava 4-nitroazobenzena Redukcija 4-nitroazobenzena Oksidacijski postupak sinteze SPEKTROSKOPSKE METODE Infracrvena spektroskopija (IR) Nuklearna magnetska rezonancija (NMR) Spektrometrija masa (MS) KVANTNO-MEHANIČKI RAČUNI...19 IV
5 SADRŽAJ 4.REZULTATI I RASPRAVA PRIPRAVA NITROAZOBENZENA Spektrometrija masa RAČUNALNI DIO Bazičnost 4-aminoazobenzena Relativne stabilnosti mogućih međuprodukata oksidacije 4-aminoazobenzena ZAKLJUČAK LITERATURNI IZVORI DODATAK... VIII 7.1. IR spektri...viii 7.2. NMR spektri... IX 7.3. MS spektar...x 8. ŽIVOTOPIS... XI V
6 SAŽETAK Sveučilište u Zagrebu Prirodoslovno-matematički fakultet Kemijski odsjek PRISTUP SINTEZI 4-NITROZOAZOBENZENA MARIJA SOKOLOVIĆ Sveučilište u Zagrebu, Prirodoslovno-matematički fakultet, Kemijski odsjek, Zavod za organsku kemiju, Horvatovac 102a, Zagreb, Hrvatska U ovom radu istraženi su različiti sintetski pristupi priprave 4-nitrozoazobenzena, poznatim metodama oksidacije i redukcije. Nijedan od pristupa sintetske priprave nije dao 4-nitrozoazobenzen. Kao produkt sinteze oksidacijskom metodom nastajao je 4-nitroazobenzen, odnosno redukcijskom metodom 4-aminoazobenzen. Kako bi se razjasnio problem, pristupilo se računalnoj metodi. Izračunata je bazičnost aminskih reaktanata s obzirom na mjesto protoniranja dušikovih atoma te relativna stabilnost mogućih produkata oksidacije 4-aminoazobenzena (odnosno redukcije 4-nitroazobenzena), kao i utjecaj supstituenata na stabilnost pojedinog spoja. Dobivene vrijednosti su razjasnili bazičnost 4-aminoazobenzena s obzirom na mjesto protoniranja dušikovih atoma, te se ujedno dobio uvid u termodinamički najstabilniji oksidacijski put 4-aminoazobenzena. Rad je pohranjen u Središnjoj kemijskoj knjižnici, Kemijski odsjek, Prirodoslovnomatematički fakultet, Sveučilište u Zagrebu, Horvatovac 102a, Zagreb, Hrvatska. (28 stranica, 26 slika, 3 tablice, 44 literaturna navoda; jezik izvornika: hrvatski) Ključne riječi: aminoazobenzen, azobenzen, bazičnost, oksidacijska metoda, redukcijska metoda, relativna stabilnost, sinteza Mentor: Prof. dr. sc. Hrvoj Vančik Neposredni voditelj: Dr. sc. Igor Rončević Ocjenjivači: Zamjena: Prof. dr. sc. Hrvoj Vančik Prof. dr. sc. Predrag Novak Prof. dr. sc. Željka Soldin Prof. dr. sc. Zlatko Mihalić Rad prihvaćen: 10. svibnja VI
7 ABSTRACT University of Zagreb Faculty of Science Department of Chemistry APPROACH TO THE SYNTHESIS OF 4-NITROSOAZOBENZENE MARIJA SOKOLOVIĆ University of Zagreb, Faculty of Science, Department of Chemistry, Division of Organic Chemistry, Horvatovac 102a, Zagreb, Croatia In this master thesis, the synthesis of 4-nitrosoazobenzene was attempted using different synthetic methods, such as oxidation and reduction methods. None of the attempted synthetic approaches gave 4-nitrosoazobenzene. The product of the oxidation method was 4-nitrosoazobenzene, while the reduction method yielded 4-aminoazobenzene. In order to clarify the problem, computational methods were used. The basicity of various nitrogen atoms of the amine reactant was estimated, as well as the relative stabilities of the possible products of oxidation of 4-aminoazobenzene (or the reduction of 4-nitroazobenzene). Also, the influence of substituents on the stability of invesigated compounds was calculated. The obtained values have clarified the preffered protonation location of the 4-aminoazobenzene, and also gave insight into its the most stable oxidation path. This Thesis is deposited in the Central Chemical Library, Department of Chemistry, Faculty of Science, University of Zagreb, Horvatovac 102a, Zagreb, Croatia. (28 pages, 26 figures, 3 tables, 44 citations; original in Croatian) Keywords: aminoazobenzene, azobenzene, basicity, oxidation method, reduction method, relative stability, synthesis Mentor : Dr. Hrvoj Vančik, Professor Direct supervisor: Dr. Igor Rončević Reviewers: Dr. Hrvoj Vančik, Professor Dr. Predrag Novak, Professor Dr. Željka Soldin, Associate Professor Subsitute: Dr. Zlatko Mihalić, Professor Thesis accepted: May 10 th, VII
8 1. UVOD Nitrozo spojevi vrlo su zanimljiva klasa spojeva za istraživanje jer bi mogli imati široku primjenu u molekulskoj elektronici i molekulskoj logici. 1 Osim toga, vrlo važna karakteristika ovih spojeva je da u čvrstom stanju pokazuju fotokromni i termokromni učinak, te stvaranje dimernih oblika (azodioksida). Dimerizacija u azodiokside i njihova povratna disocijacija u nitrozo-spojeve mogla bi se primijeniti za konstrukciju novih supramolekulskih struktura čije bi građevne jedinice bile nitrozo monomeri. 2 Derivati azobenzena su zadnjih desetljeća intenzivno proučavani i eksperimentalno i teoretski, budući da imaju mogućnosti široke primjene u reverzibilnim optičkim uređajima za pohranu podataka (holografskim i digitalnim). 2 Osim ove primjene, derivati azobenzena korišteni su i kao spektrofotometrijske probe i kao kiselo-bazni indikatori u analitičkoj kemiji budući da protoniranjem, odnosno deprotoniranjem, dolazi do vidljivih promjena boje otopine. 2 Kombinacija azo-skupine i nitrozo-skupine u istoj molekuli činile bi sustav u kojem bi se dimerizaciju i disocijaciju nitrozo funkcije moglo kontrolirati fotoizomerizacijom azoskupine. Prva faza ovog istraživanja i cilj ovog rada bio je pristup sintetskoj pripravi nitrozoazobenzena, spoja s dvije fotokromne skupine, nitrozo i azo skupinom. Iskušani su raznovrsni sintetski pristupi, koji se temelje na oksidaciji amina. Budući da standardnim oksidacijskim metodama nije nastao djelomično oksidirani nitrozo već potpuno oksidirani nitro derivat, pokušali smo računalnim metodama rastumačiti razloge za takvo ponašanje. Izračunata je bazičnost aminskih reaktanata s obzirom na mjesto protoniranja dušikovih atoma te relativna stabilnost mogućih produkata oksidacije 4-aminoazobenzena (odnosno redukcije 4-nitroazobenzena), kao i utjecaj supstituenata na stabilnost pojedinog spoja. 1
9 2. LITERATURNI PREGLED 2.1. SVOJSTVA NITROZO SPOJEVA Aromatski nitrozo spojevi C-nitrozo spojevi poznati su više od stotinu godina u obliku plavih ili zelenih otopina, odnosno bezbojnih ili bijelih kristala. Pokazalo se da zapravo postoje dva različito obojena oblika istog spoja monomer i dimer. 2 Razvitkom IR spektroskopije dokazano je postojanje i dva dimerna oblika aromatskih nitrozo spojeva: trans- tj. E-dimer i cis- tj. Z-dimer (Shema 1). 3 Shema 1. Dimerizacija nitrozo spojeva. Prelazak jednog izomera u drugi se odvija preko monomernog oblika, što znači da ne dolazi do izravne cis-trans izomerizacije. 4 E-dimer je najstabilniji u čvrstom stanju zbog svoje centrosimetričnosti. 2 U otopinama na sobnoj temperaturi prevladava plavi/zeleni monomer, a hlađenjem otopine uspostavlja se ravnoteža monomer-dimer pri čemu Z-dimera ima nešto više nego E-dimera. 2 Nitrozo spojevi koji se u čvrstom stanju pojavljuju kao monomeri često su aromatski nitrozo spojevi sa supstituentima s jakim elektron-donorskim djelovanjem ( OR ili NR 2 ) vezanima u para-položaj. Ostali para-supstituenti sa slabim elektron-donorskim ili elektronakceptorskim utjecajem pospješuju stvaranje dimera. U orto-položaju su prisutne steričke smetnje supstituenata i kisika te dolazi do izvrtanja fenilnih prstenova izvan ON-NO ravnine ili ne dolazi do dimerizacije. Glavni razlog što neki nitrozo-spojevi ne dimeriziraju, čak ni širokom varijacijom reakcijskih uvjeta, može se protumačiti velikim doprinosom rezonantne strukture opisane na Shemi 2. To tumačenje proizlazi iz istraživanja dinamičkom NMR spektroskopijom kojom se može izmjeriti rotacijska barijera za rotaciju oko C-N veze. Visoka rotacijska barijera posljedica je jednostruke CN veze s parcijalnim karakterom dvostruke veze kakva proizlazi iz 2
10 navedenih rezonantnih struktura. Za N-supstituirane 4-nitrozoaniline opaženo je da imaju višu energijsku barijeru za rotaciju nitrozo skupine oko veze C-N od ostalih 4-supstituiranih spojeva. 5 Visoka energijska barijera za rotaciju nitrozo skupine ukazuje, dakle, na veliki doprinos kinoidne rezonantne strukture (Shema 2). 6 Shema 2. Kinoidna rezonancijska struktura para- supstituiranih aromatskih nitrozo spojeva. Neki od nitrozo-spojeva su i u čvrstom stanju postojani u više od jednog oblika, mogu se izolirati i kao monomer i kao dimer. Jedan od takvih spojeva je 4-jodnitrozobenzen. 7 Razlog za monomerne kristale 4-jodnitrozobenzena je u načinu kristalnog pakiranja u kojem se u susjedstvu nalaze nitrozo skupina i atom joda, a ne dvije nitrozo skupine, što bi bio uvjet za dimerizaciju Alifatski nitrozo spojevi Alifatski nitrozo spojevi, koji sadrže vodik na α-ugljikovom atomu uz nitrozo skupinu lako se pregrađuju u oksime. 8,9 Tijekom te ireverzibilne termičke pregradnje dolazi do [1,3]-pomaka vodika na kisikov atom (Shema 3). Shema 3. Pregradnja nitrozo spojeva u oksime. U oksime se, osim nitrozo-spojeva koji nemaju α-vodik uz NO skupinu, ne pregrađuju ni oni koji imaju velike alkilne skupine i nepovoljnu geometriju. 10 3
11 Priprava nitrozo spojeva Nitrozo spojevi vrlo su reaktivni. Iz tog razloga se npr. neki amino spoj oksidacijom u nitrozo, može vrlo lako dalje oksidirati u nitro spoj, prilikom čega dolazi do smanjenja iskorištenja reakcije. Stoga, vrlo je važan odabir oksidacijskog sredstva kao i uvjeti pod kojima se odvija sama reakcija. Sve navedeno je rezultiralo razvojem velikog broja metoda sinteze i uporabom različitih reagensa Oksidacijske metode Korištenjem odgovarajućih reagensa, određeni primarni aromatski amini mogu se oksidirati u nitrozo spojeve. Neki od najčešće korištenih oksidansa su: Carova kiselina, tj. peroksimonosumporna kiselina (H 2 SO 5 ) prikazana na Shema 4, zatim peroctena kiselina, kalijev permanganat, 3-kloroperoksibenzojeva kiselina (MCPBA) i peroksimravlja kiselina. Često se koristi i vodikov peroksid uz akvaheksametilfosforamidoksodiperokso molibden(vi), MoO(O 2 ) 2 (H 2 O)(hmpa) za aromatske amine. 11 Shema 4. Dobivanje nitrozo spojeva oksidacijom amina. Jedan od novijih i vrlo djelotvornih reagensa za oksidaciju je kompleks [MoO(O 2 ) 2 (H 2 O)(hmpa)]. 12 On se priređuje iz molibdenovog(vi)oksida, heksametilfosforamida i vodikovog peroksida. 13 Za oksidaciju se mogu primijeniti i natrijev perborat 14 ili Na 2 WO 4 H 2 O Međutim, najbolji rezultat su dobiveni koristeći kalijev peroksimonosulfat, poznat pod nazivom Oxone, 2KHSO 5 KHSO 4 K 2 SO Redukcijske metode Aromatski nitro spojevi mogu se reducirati do amina jačim reducensima (Sn; SnCl 2 + HCl; Fe + HCl; H 2 + Pt). Uporabom slabijih reducensa i kontroliranjem koncentracije ph otopine, mogu se izolirati i nitrozo spojevi i hidroksilamini kao produkti izravne redukcije ili sekundarnih reakcija. 16 4
12 Odgovarajući nitro spojevi (RNO 2 ) mogu se reducirati uz pomoć cinka u prahu i amonijeva klorida do aril/alkilhidroksilamina (RNHOH). 16 Bez izoliranja iz reakcijske smjese, dobiveni spojevi se kontroliranom reakcijom oksidiraju otopinom željezovog(iii) klorida u derivate nitrozobenzena, pri čemu se još kao drugi oksidans može upotrijebiti i kisela otopina natrijevog bikromata (Shema 5), a moguće je koristiti i kalijev heksacianoferat(iii) u natrijevoj lužini te perjodate ili srebrov karbonat (Ag 2 CO 3 pokazuje jako dobra iskorištenja pri čemu se izbjegava stvaranje azoksi derivata reakcijom nitrozo spoja i zaostalog hidroksilamina). 11 Shema 5. Redukcija nitro spoja do hidroksilamina, nakon čega slijedi oksidacija hidroksilamina u odgovarajući nitrozo derivat. Također je moguća i priprava nitrozo spojeva metodoma direktne adicije NO + iona. Jedna od takvih metoda je adicija NOX ili klornitrozo-adicija. Adicijom NOCl na alkene mogu se dobiti tri produkta. 2 Početni produkt uvijek je β-halonitrozo-spoj (Shema 6), koji je stabilan samo ukoliko ugljikov atom direktno vezan na dušik nema vodikovih atoma. U suprotnom, nitrozo-spoj tautomerizira u oksim. Kod određenih alkena, početni β-halonitrozospoj se oksidira s NOCl u β-halonitro-spoj. Reakcije adicije mogu se odvijati i uz druge funkcionalne skupine (npr. COOH, COOR, CN, OR) i to jednostavnom elektrofilnom adicijom, najčešće anti, iako su nađeni i slučajevi syn adicije. 2 Reakcija slijedi Markovnikovljevo pravilo, NO + odlazi na ugljik s više vodikovih atoma. Shema 6. Priprava nitrozo spoja direktnom redukcijom. 5
13 2.2. AZO SPOJEVI Izomeri azobenzena (trans- (tab) i cis- (cab)), kao i njihovi supstituirani derivati su zadnjih desetljeća proučavani i eksperimentalno i teoretski zbog svoje široke primjene. Pokazuju sposobnost trans-cis fotoizomerizacije. Četiri su moguća mehanizma: rotacija, inverzija, usklađena inverzija te inverzija uz pomoć rotacije (Shema 7), koja uključuje rotaciju (torziju ili izvijanje) oko centralne N=N veze uz nužno kidanje π veze. Rotacijom se mijenja C-N-N torzijski kut dok N-N-C kut ostaje fiksiran na oko 120. U inverzijskom mehanizmu, N=N-C kut se povećava na 180, dok C-N=N-C kut ostaje oko 0, što rezultira u prijelaznom stanju s jednim sp- hibridiziranim azo dušikovim atomom. U usklađenoj inverziji, oba N=N-C vezna kuta se povećavaju na 180 uz generiranje linearnog prijelaznog stanja. U inverziji pomoću rotacije dolazi do velike promjene u C-N=N-C kutu i do manje, ali značajne istovremene promjene N=N-C kuta. Prijelazno stanje nastalo u usklađenoj inverziji nema ukupni dipolni moment, dok preostala tri mehanizma karakterizira polarno prijelazno stanje. Relaksacijom sva četiri prijelazna stanja može se dobiti cis- ili trans- izomer; dakle sva četiri mehanizma predvođena fotostacionarnim stanjem sadrže oba izomera. Eksperimentalna opažanja se u većini slučajeva objašnjavaju upravo tim više izomerizacijskim putevima. 17 Shema 7. Mehanizmi izomerizacije azo spojeva. 6
14 Aminoazobenzeni Većina derivata 4-aminazobenzena je intenzivno obojeno. To svojstvo im omogućuje primjenu u pripravi sintetičkih boja koje se koriste u proizvodnji tekstila kao i agrokemijskoj i farmaceutskoj industriji. Azobenzeni koji sadrže amino ili dialkilamino skupinu podložni su izrazitoj promjeni boje u otopini ili polimernom filmu uslijed protoniranja. U molekuli 4-aminoazobenzena dva su glavna bazična centra na β dušiku i na amino dušiku. Rogers, Cambell i Maatmann 18 su zaključili kako se tijekom protoniranja prvi proton adira na β dušik, dok su Klotz 19 i suradnici ispitivanjem bazičnosti derivata 4- aminoazobenzena zaključili da se prvi proton adira na amino dušik (Shema 8). Dakle, ne postoji suglasje o relativnoj bazičnosti dušikovih atoma 4-aminoazobenzena. Shema 8. Moguća mjesta protoniranja 4-aminoazobenzena. 7
15 2.3. SPEKTROSKOPSKE METODE U PROUČAVANJU NITROZO I AZO SPOJEVA IR spektroskopija Najčešće primjenjivana metoda za razlikovanje monomernih te E- i Z- dimernih oblika azodioksida je infracrvena spektroskopija. 7 Alifatski nitrozo monomeri imaju karakteristične signale u području cm -1, dok aromatski spojevi imaju signale kod nižih valnih brojeva: cm 1. Aromatski E-dimeri mogu se karakterizirati vrlo jakom apsorpcijom u području cm 1 koja odgovara antisimetričnom rastezanju ON=NO skupine. Simetrično rastezanje nije aktivno u infracrvenom spektru, već se može vidjeti tek u Ramanovom spektru. Aromatski Z-dimer pokazivat će dva signala pri 1410 cm 1 i 1395 cm 1, koji odgovaraju simetričnom i antisimetričnom rastezanju N 2 O 2 skupine. 25 Rastezanja jednostrukih C-N veza kod dimera javljaju se oko 845 cm 1, a kod monomera oko 825 cm 1. U IR spektru mogu se vidjeti i deformacije CNO kuta oko 474 cm 1 kod monomera i oko 418 cm 1 kod dimera. 7 IR spektri aromatskih azo-spojeva mogu se okarakterizirati vrlo jakom apsorpcijom u području 1445 cm -1, koja odgovara asimetričnom istezanju -N=N- skupine UV/VIS spektroskopija Jedna od prvih metoda kojom su bili proučavani nitrozo spojevi i praćene njihove ravnoteže u otopini bila je UV/VIS spektroskopija. Plava, odnosno zelena boja nitrozo monomera potječe od n π* prijelaza slobodnog elektronskog para lokaliziranog na dušikovom atomu. 20 Apsorpcijske n π* vrpce u UV/VIS spektru azodioksi dimera nema, jer taj slobodni elektronski par tvori N=N vezu (Shema 9). Shema 9. Nastajanje azodioksi dimera. Svojstva azobenzena, odnosno azo skupine, u neutralnoj i kiseloj sredini su istraživana UV/VIS spektroskopijom. Spektri protoniranih trans-ab i cis-ab se međusobno razlikuju. Protoniranjem vrpce nižih valnih brojeva koje odgovaraju n!π * prijelazu nestaju dok druge 8
16 vrpce pokazuju crveni pomak. Trans- konjugirane kiseline azobenzena su planarne dok cisizomeri gube C 2 os simetrije i postaju asimetrični. U slučaju trans- azobenzena i njegove konjugirane kiseline tabh*, usporedbom geometrije zaključeno je da protoniranjem dolazi do produljenja N=N veze, skraćivanja C-N veze i promjene pridruženog veznog kuta C-N veze te različite zakrivljenosti fenilnih prstenova. Kod cis-azobenzena također dolazi do produljenja N=N veze, ali se skraćuje samo N 2 C 4 veza. Protoniranjem jedan benzenski prsten ostaje nepromijenjen, a torzijski kut između benzenskog prstena i N=N- veze ne mijenja se značajno, dok kod drugog benzenskog ' prstena se gotovo vidi koplanarnost s N=N skupinom. 21 Apsorpcijski spektar azobenzena u vidljivom i bliskom ultraljubičastom području određen je (n! π * ) vrpcama između 380 i 520 nm i (π! π * ) vrpcama na 330 nm (trans-) i 275 nm ( cis-) H i 13 C NMR spektroskopija Nitrozo-spojevi proučavani su 1 H i 13 C NMR spektroskopijom u različitim otapalima u širokom rasponu temperatura. 6 Pri sobnim temperaturama u NMR spektrima se vide samo signali monomera, dok pri nižim temperaturama u otopinama postoje oba dimerna oblika u ravnoteži s monomerom. Zadnjih 30 godina intenzivno je bila istraživana ograničena rotacija nitrozo-skupine oko CN veze u aromatskim nitrozo spojevima. 4 Na nižim temperaturama (223 K) rotacija je toliko usporena da se mogu razlikovati ortho-vodikovi atomi na C2 i C6 položajima u 1 H NMR spektrima. 23 Otkriveno je i da nesimetrični ortho-supstituirani nitrozobenzeni mogu postojati kao stabilni konformeri. 24 Protoni koji su u ortho-,meta-,parapoložaju na istoj strani prema nitrozo-skupini pokazuju neobično visoke vrijednosti kemijskog pomaka, a oni na suprotnoj strani izrazito niske vrijednosti kemijskog pomaka. 24 Nakon uspostavljanja ravnoteže, azobenzen postoji isključivo kao trans-izomer. To je vidljivo analizom NMR spektra, koji pokazuje tri skupa signala što odgovara protonima u položajima 4, 3 i 5 te 2 i 6. Brza rotacija oko N-C 1 veze čini atome u položajima 3 i 5 te 2 i 6 ekvivalentnima. Dva fenilna prstena azobenzena kemijski su ekvivalentni, a parovi protona i ugljikovih atoma dijele kemijske pomake (Slika 1). 25 9
17 Slika 1. Magnetno ekvivalentni ugljikovi atomi azobenzena. Utjecaj J J sprezanja rezultira cijepanjem signala: signal za protone u položajima 4 i 4' je triplet intenziteta 2 s pomakom na 7,09 ppm, signal za protone u položaju 3 i 5 te 3' i 5' je triplet intenziteta 4 s pomakom na 7,17 ppm, a signal za protone u položajima 2 i 6 te 2' i 6' je je dublet intenziteta 4 s pomakom na 8,02 ppm. Očekuje se da 1 H NMR spektar cisazobenzena bude identičan samo s različitim pomacima. Tako za protone u položajima 4 i 4' kemijski pomak iznosi 6,70 ppm, za protone u položajima 3 i 5 te 3' i 5' 6,81 ppm, dok za protone u položajima 2 i 6 te 2' i 6' kemijski pomak iznosi 6,68 ppm. 10
18 2.4. FOTOKROMIZAM I TERMOKROMIZAM NITROZO I AZO-SPOJEVA Fotokromizam (od grč. phos (svjetlo) i khroma (boja)) je pojava promjene boje neke tvari prouzročena elektromagnetskim zračenjem. 26,27 Taj se proces može opisati kao transformacija spojeva (Shema 10) koji imaju različite apsorpcijske spektre. Shema 10. Fotokromizam. Ako je ista pojava izazvana toplinom govorimo o termokromizmu (od grč. therme). 3 Fotokromni i/ili termokromni učinak pojavljuje se u otopinama, no u čvrstoj fazi je rjeđi. Fokromizam u kristalima i polikristalima je posebno zanimljiv jer bi se mogao primijeniti u optoelektronskim uređajima kao optičke memorije i optoelektronički prekidači. Otkriveno je da fotokromni i termokromni učinak u čvrstom stanju pokazuju različiti ciklički i biciklički spojevi. Aromatski nitrozo-spojevi također pokazuju takav efekt u različitim sustavima. 27, Fotokromizam i termokromizam nitrozo spojeva u čvrstom stanju Nitrozo spojevi kao fotokromni sustavi bili su poznati u otopinama, stoga se pretpostavilo da će pokazivati fotokromno i termokromno ponašanje i u čvrstom stanju (Shema 11). 29 Shema 11. Fotokromno, odnosno termokromno ponašanje nitrozo spojeva. Vidljivom razlikom u boji između monomera (plavi, apsorbira oko 650 nm) i dimera (žuti ili bezbojan, apsorbira oko 290 nm) zadovoljen je uvjet fotokromizma reaktanti i produkti apsorbiraju pri bitno različitim valnim duljinama Ravnoteže monomer-dimer nitrozo-spojeva bile su proučavane u otopinama, a vizualnim praćenjem obojenja moguće je bilo utvrditi i nastanak monomera. 33 Većina nitrozo-spojeva se u čvrstom stanju nalazi u 11
19 obliku azodioksidnih dimera. Izuzetak su sterički ometani nitrozobenzeni i spojevi s jakom elektron-donirajućom skupinom u para- položaju. Tako se N-supstituirani nitrozoanilini u čvrstom stanju pojavljuju kao monomeri. 4 Fotokromizam azobenzena u otopini ovisi o prirodi otapala i osjetljiv je na prisutnost katalitičkih spojeva. Ta osjetljivost se pripisuje supstituenskim skupinama na fenilnim prstenovima azobenzena. Primjerice, azobenzen i 4-aminoazobenzen imaju slična fotokromna svojstva u ugljikovodičnim i vrlo suhim alkoholima. No, ukoliko je nazočna veća količina vlage, mijenja se brzina cis-trans pretvorbe u tami. Aminoazobenzeni bez N-alkiliranih supstituenata nisu fotokromni u vodi i u vrlo jakim lužinama. 34 Otapala s hidroksilnim skupinama (voda, alkoholi i njihove smjese) destabiliziraju cis-izomere. Vjerojatan uzrok destabilizacije cis-oblika aminoazobenzena otapalima s hidroksilnom skupinom je nazočnost protona, a ne samo priroda otapala. Fotokromizam azobenzena ima vrlo široku primjenu, primjerice, za foto uređivanje u membranama i kontrolu viskoznosti polimera
20 3. EKSPERIMENTALNI DIO 3.1. MATERIJALI Za sintezu nitrozoazobenzena korišteni su navedeni materijali: 1. 4-aminoazobenzen, C 12 H 11 N 3 (Sigma Aldrich) 2. Oxone, 2KHSO 5 KHSO 4 K 2 SO 4 (Sigma Aldrich) 3. Natrijev hidrogenkarbonat, NaHCO 3 (Kemika) 4. Diklormetan, DCM 5. p-nitronitrozobenzen, C 6 H 4 N 2 O 3 6. Anilin, C 6 H 7 N 7. Octena kiselina, C 2 H 4 O 2 8. m-klorperbenzojeva kiselina, C 7 H 5 ClO 3 (Sigma Aldrich) 9. Bezvodni natrijev sulfat, Na 2 SO 4 (Kemika) 10. Kalijev bromid, KBr (Sigma Aldrich) Za praćenje tijeka reakcija u otopini i uvid u čistoću spojeva korištena je tankoslojna kromatografija (TLC) na pločicama silikagela (60 Å, 200 µm, 254 nm, Fluka). Za pročišćavanje spojeva kromatografijom na stupcu korišten je silikagel (90 Å, φ , Sigma Aldrich). 13
21 3.2. POKUŠAJI PRIPRAVE NITROZOAZOBENZENA Priprava 4-nitronitrozobenzena Otopini Oxone-a (40,87 g; 66,05 mmol) u vodi (405 cm 3 ) uz miješanje se dokapava otopina 4- nitroanilina (4,09 g; 29,6 mmol) u diklormetanu (105 cm 3 ). Nakon 1,5 sat sav 4-nitroanilin je izreagirao te se miješanje zaustavi. Diklormetan se upari, a dobivena smjesa se dalje koristi za pripravu 4-nitroazobenzena (3.2.2.) Priprava 4-nitroazobenzena Pripravljena smjesa 4-nitronitrozobenzena (3,3706 g; 22,16 mmol) se otopi u octenoj kiselini (15 cm 3 ) te se uz miješanje doda anilin (120 cm 3 ). Reakcija se odvija 5 dana. Octena kiselina se upari. Pročišćava se 295 mg smjese kromatografijom na stupcu silikagela u diklormetanu (Slika 3). Dobiveno je 211,4 mg (49%) crvenonarančastih kristala 4-nitroazobenzena (Slika 2). Slika 2. Sintetizirani 4-nitroazobenzen kondenzacijom anilina i p-nitronitrozobenzena. Spektroskopska karakterizacija sintetiziranog spoja IR (KBr) valni broj/ cm -1 : 687, 859, 1344, Redukcija 4-nitroazobenzena 4-nitroazobenzen (167 mg; 0,7368 mmol) se otopi u vodi 1,2-dimetoksietanu (4,2 cm 3 ) te se uz miješanje doda amonijev klorid (0,065 g; 1,22 mmol). Zatim se doda cink (0,28 g; 4,28 mmol) koji je prethodno aktiviran s 0,5 mol dm -3 HCl te ispran s vodom, etanolom, acetonom 14
22 i eterom. Reakcija se prati na TLC pločici u otapalu diklormetanu. Nakon 2h izreagira gotovo sav 4-nitroazobenzen. Zelenonarančasta smjesa se profiltrira i ispere s 1,2-dimetoksietanom kako bi se uklonio nastali bijeli talog cinkova oksida. U ohlađeni filtrat se doda otopina FeCl 3 x6h 2 O (0,26 g; 1,38 mmol). Nastala zelenosmeđa smjesa se ekstrahira tri puta diklormetanom. Sakupljeni organski ekstrakti se suše na bezvodnom natrijevom sulfatu. Nakon uparavanja diklormetana, dobivena smjesa produkata pročišćava se kromatografijom na stupcu silika-gela, a kao eluens se koristi diklormetan (Slika 3). Slika 3. Odvajanje pripravljenih 4-nitroazobenzena (lijeva kolona), odnosno 4-aminoazobenzena (desna kolona) kromatografijom na stupcu silikagela. Dobiveno je 46 mg zelenonarančastog spoja. Iskorištenje reakcije iznosi 27, 55 %. Spektroskopska karakterizacija sintetiziranog spoja IR (KBr) valni broj/ cm -1 : 770, 801, 1020, 1096, 1139, 1261, 1306, 1415, 1505, 1597, 1617, 2963, H NMR (400 MHz, CDCl 3 ) δ / ppm: 7,850; 7,505; 7,428; 7,284; 6,702; 4,
23 Oksidacijski postupak sinteze a) U okrugloj tikvici se pomiješa 120 mg 4-aminoazobenzen i Oxone-a u omjeru 1:2. Prethodno se 4-aminoazobenzen otopi u diklormetanu, a zatim se doda natrijev hidrogenkarbonat te uz snažno miješanje dokapava Oxone otopljen u vodi. Reakcija se prati na TLC pločici. Nakon izreagiranog polaznog spoja, smjesa se profiltrira i ekstrahira tri puta diklormetanom. Organski sloj se suši na bezvodnom natrijevom sulfatu. Otapalo se upari. Dobiven je produkt narančaste boje. Dobiveno je 21 mg spoja. Iskorištenje reakcije iznosi 17,5 %. Intenzivan pik na 3343 cm -1 potječe od vlage. Spektroskopska karakterizacija sintetiziranog spoja IR (KBr) valni broj/ cm -1 : 687, 859, 1344, H NMR (400 MHz, CDCl 3 ) δ / ppm: 8,129; 8,076; 7,994; 7,578; 7, C NMR (100 MHz, CDCl 3 ) δ/ ppm: 124,7; 129,3; 147,8 ; 152,4; 155,5. b) Mehanokemijska sinteza obuhvaćala je metodu kojom se 4-aminoazobenzen i Oxone usitnili i miješali mljevenjem. Mljevene je provedeno u mlinu, u posebnim čeličnim ili teflonskim posudicama u koje se osim polaznog spoja stavljene i kuglice određenog promjera. Uloga kuglica je da miješaju reaktante te prijenosom mehaničke energije potiču reakciju. Proces usitnjavanja je bitan za mehanokemijsku sintezu jer jedan od modela kojim se objašnjavaju reakcije provedene mehanokemijski jest difuzija reaktanata. Kada se dva reaktanta nađu jedan kraj drugoga, dolazi do difuzije molekula kroz same slojeve reaktanata te se na dodirnoj površini stvara sloj produkta. Osim homogenizacije uzorka, uslijed mljevenja dolazi i do povećanja specifične površine reaktanata. Veća specifična površina ubrzava reakciju. 36 Osim modela difuzije čestica, još dva glavna modela koji pokušavaju opisati mehanokemijske reakcije su teorija vruće točke (eng. hot spot theory), koja se oslanja na trenje i magma-plazma model, koji uzima u obzir direktne udarce kuglica i metala, a ne trenje. 36 Nakon 30 min spoj je izoliran u diklormetanu. Nakon uparavanja diklormetana, dobivena smjesa produkata pročišćava se kromatografijom na stupcu silika-gela, a kao eluens se koristio diklormetan. 16
24 Spektroskopska karakterizacija sintetiziranog spoja IR (KBr) valni broj/ cm -1 : 687, 859, 1344, H NMR (400 MHz, CDCl3) δ / ppm: 8,129; 8,076; 7,994; 7,578; 7, C NMR (100 MHz, CDCl3) δ/ ppm: 124,7; 129,3; 147,8; 152,4; 155,5. c) U okrugloj tikvici pomiješa se 4-aminoazobenzen i m-klorperbenzojeva kiselina (1:1) u diklormetanu. Reakcija se provodi 20 minuta, a tijek reakcije se prati sustavom plinska kromatografija spektrometrija masa na početku reakcije, nakon 5 min, 10 min i 20 min, spektrometrom masa. Dobiveni spektri uspoređeni su sa spektrima iz baze podataka. Spektroskopska karakterizacija spoja m/z: 227, 213, 197, 105, 92, 77, 65,
25 3.3. SPEKTROSKOPSKE METODE Infracrvena spektroskopija (IR) IR spektri snimljeni su FTIR spektrometrom Perkin Elmer Spectrum Two te analizirani pomoću programskog paketa Perkin Elmer Spectrum V10. Uzorci su pripremani tehnikom KBr pastile (KBr:spoj = 100:1). KBr se pomiješao s uzorkom u navedenom omjeru i usitnio u ahatnom tarioniku, a zatim se prešao u pastilu. Spektri su snimani u području od 4000 do 400 cm -1 uz spektralno razlučivanje od 4 cm Nuklearna magnetska rezonancija (NMR) NMR spektri snimljeni su na Bruker Ascend 400 spektrometru pri konstantnom magnetskom polju od 9,4 T u NMR cjevčicama promjera 5 mm pri 298 K. Spektri su snimljeni prema TMS-u kao unutarnjem standardu, a kao otapalo korišten je deuterirani kloroform (CDCl 3 ). Za snimanje 1 H NMR spektara korištena je spektralna širina od 6 khz, uz relaksacijsko vrijeme odgode od 1 s te vrijeme akvizicije u rasponu od 2,73 do 5,31 s. Broj pulseva po spektru bio je 32. Digitalno razlučivanje iznosilo je od 0,18 do 0,37 Hz po točki Spektrometrija masa (MS) Za analizu produkta dobivenog oksidacijom s MCPBA korišten je vezani sustav plinska kromatografija-spektrometar masa. Uzorak otopljen u CH 2 Cl 2 je injektiran u plinski kromatograf Varian 3800 GC. Kao plin nosioc korišten je He. Temperatura kolone varirala je u rasponu od C, a protok je iznosio 1 ml/ min. Kao detektor je korišten spektrometar masa. Analiza je provedena na uređaju Saturn 2200 GC/MS/ MS. 18
26 3.4. KVANTNO-MEHANIČKI RAČUNI Svi računi provedeni su korištenjem programskog paketa Gaussian Optimizacije geometrija i frekvencijski računi provedeni su prvo na osnovnom skupu 6-31G(d,p), nakon čega su strukture reoptimizirane korištenjem osnovnog skupa G(2d,p) uz ključnu riječ int=ultrafine. Gibbsove energije zatim su izračunate frekvencijskim računima provedenim na istoj razini teorije. Isprobani su B3LYP, M06-2X i ωb97x-d funkcionali. Kao model implicitnog otapala korišten je SMD. 42 U slučajevima dodavanja jedne eksplicitne molekule vode, ona je dodana ručno na način da stupa u najjaču vodikovu interakciju s proučavanim spojem. 19
27 4.REZULTATI I RASPRAVA 4.1. PRIPRAVA NITROAZOBENZENA Jedan od osnovnih ciljeva ovog rada bio je istražiti mogućnosti sinteze nitrozoazobenzena. Korištene su i metode temeljene na redukciji i na oksidaciji, a svi iskušani sintetski pristupi prikazani su u Tablici 1. Osim Oxone-a, kao oksidans korištena je i m-klorperbenzojeva kiselina kao slabiji oksidans. Za redukciju je pripravljen 4-nitroazobenzen, kondenzacijom anilina i p-nitronitrozobenzena (Shema 12). Tablica 1. Sinteze provedene tijekom ekperimentalnog rada. Prilikom ponavljanja istih eksperimenata varirano je vrijeme i omjer koncentracija reaktanata. Broj i vrsta sinteze Polazni spoj Oksidacijsko (redukcijsko) sredstvo Produkt(i) sinteze n;t; komentar* 1.Otopinska sinteza 4-aminoazobenzen Oxone 4-nitroazobenzen 3; Mehanokemijska sinteza 4-aminoazobenzen Oxone uz dodatak NaHCO 3 4-nitroazobenzen 3; sobna Oxone 4-aminoazobenzen 3; sobna 3.Otopinska sinteza 4. Otopinska sinteza 5.Otopinska sinteza 6.Otopinska sinteza 4-aminoazobenzen bromidna sol 4-aminoazobenzena 4-aminoazobenzen 4-nitroazobenzen vodikov peroksid uz MoO 3 kao katalizator Oxone m-klorperbenzojeva kiselina 1.cink 2. željezov(iii)klorid heksahidrat 4-aminoazobenzen 4-nitroazobenzen, 4-aminoazobenzen (smjesa) 4-nitroazobenzen, 4-aminoazobenzen (smjesa) 1. 4-hidroksilaminoazobenzen 2. 4-aminoazobenzen 1; sobna; prema ref. 44 1; sobna; problematična izolacija 2; sobna i 273; problematična izolacija, analiza MS 4; 273; zeleno obojenje *n označava broj ponovljenih eksperimenata, a T temperaturu u Kelvinima. Otopinska sinteza s oksonom rađena u omjerima 1:4 i 1:2 u korist oksidansa, dok je u reakciji s 3-klorperbenzojevom omjer bio 1:1. 20
28 Shema 12. Nastajanje 4-nitroazobenzena kondenzacijom anilina s p-nitronitrozobenzenom. Pripravljeni 4-nitroazobenzen dalje je reduciran kako bi se dobio željeni 4-nitrozoazobenzen. Redukcija se provodila cinkom do 4-hidroksilaminoazobenzena. Za daljnju oksidaciju do željenog 4-nitrozoazobenzena korišten je željezov(iii)klorid heksahidrat. Smeđa otopina je oksidacijom poprimila zelenu boju, koja se vrlo brzo izgubila nakon čega je smjesa poprimila crveno-smeđu boju. Kao produkt sinteze dobiven je 4-aminoazobenzen (Shema 13). Shema 13. Redukcijski pristup sintezi nitrozoazobenzena. Drugi pristup sintezi nitrozoazobenzena bila je oksidacija 4-aminoazobenzena s Oxone-om kao oksidansom, dakle klasični oksidacijski postupak koji je u većini slučajeva uspješan. Produkt takve sinteze nije bio očekivani nitrozoazobenzen, već nitroazobenzen (Shema 14). Shema 14. Nastajanje 4-nitroazobenzena reakcijom oksidacije 4-aminoazobenzena Oxone-om. 21
29 Budući da je sinteza s Oxone-om bila neuspješna, promijenjen je oksidans. Umjesto Oxone-a korištena je m-klorperbenzojeva kiselina. U takvoj sintezi kao glavni produkt dobiven je nitroazobenzen, isto kao i u slučaju s Oxone-om. Za razliku od prethodnih sinteza, u ovom radu je za uvid u strukturu spoja korišten vezani sustav GC-MS Spektrometrija masa Spoj koji se želio analizirati se pri unošenju u kromatografski sustav preveo u plinovito stanje i ispirao s kromatografske kolone inertnim plinom. Pokretna faza je plin nosilac koji ne reagira s molekulama analita već ih samo prenosi kroz kolonu. Takvim sustavom sastojci smjese odjeljuju se plinskom kromatografijom, a detektiraju spektrometrom masa. Vrlo brza analiza uz pomoć spektrometra mase kao detektora, u vezanom sustavu GC-MS, potvrdila je nastanak 4-nitroazobenzena oksidacijom s MCPBA iz 4-aminoazobenzena kao polaznog spoja. Omjer m/z matičnog iona iznosio je 227, što odgovara molekulskoj masi dobivenog produkta. Snimljeni maseni spektar nalazi se u prilogu
30 4.3. RAČUNALNI DIO Računalni pristup korišten je s ciljem rješavanja dva problema. Prvo, procijeniti bazičnost pojedinih dušikovih atoma u 4-aminoazobenzenu, budući da dostupni podaci iz literature o tome daju oprečne rezultate (vidjeti ). 18,19 Procjena relativnih bazičnosti vrlo je važna sa sintetskog aspekta, jer protoniranje nekog dušikovog atoma (i nastanak pozitivnog naboja) otežava njegovu oksidaciju. Drugo, analizirali smo relativne stabilnosti mogućih produkata oksidacije, utjecaj supstituenta, te utjecaj geometrije (cis-trans izomerije) na relativnu stabilnost mogućih produkata Bazičnost 4-aminoazobenzena Prema istraživanju Rogersa bazičniji je β-dušikov atom 18, dok je prema Klotzu 19 bazičniji dušik amino skupine. U radu su proučavane sve tri moguće protonirane strukture, što je prikazano na Slici 4. Brojevi 1, 2 i 3 označavaju moguća mjesta protoniranja. Za računanje pk b vrijednosti korištena je metoda usporedbe s referentnom strukturom. 37 Kao referentni spoj korišten je anilin. Vrijednosti pk b računate su prema jednadžbi (3). pk b (X) = pk b (X) rač pk b (anilin) rač +pk b (anilin) eksp (3) Slika 4. Moguća mjesta protoniranja 4-aminoazobenzena. 23
31 Izračunate pk b vrijednosti prikazane su u Tablici 2. Dodatak jedne eksplicitne molekule vode nema veliki utjecaj na položajima 1 i 2, ali značajan je u slučaju položaja 3. Rezultati sugeriraju da su bazičnosti 1 i 3 slične (unutar 1,5 vrijednosti pk b ), što je očekivano s obzirom na protuslovne podatke iz literature. 18,19 Promjena konformacije u cis- smanjuje sve pk b vrijednosti u rasponu od 1-1,7. Tablica 2. Izračunate pk b vrijednosti 4-aminoazobenzena. Vrsta SMD/M06-2X/6-311+G(2d,p) SMD/M06-2X/6-311+G(2d,p) + 1 H 2 O Anilin Aminoazobenzen (1) Aminoazobenzen (2) Aminoazobenzen (3) cis- Aminoazobenzen 10.5 (1) cis- Aminoazobenzen 11.4 (2) cis- Aminoazobenzen (3) Relativne stabilnosti mogućih međuprodukata oksidacije 4-aminoazobenzena Razmatramo li oksidaciju aminoazobenzena, moramo uzeti u obzir dvije mogućnosti, koje su prikazane na Slici 5. lika 5. Moguća mjesta protoniranja 4-aminoazobenzena. Svi spojevi u istom stupcu leže na istoj plohi potencijalne energije. S 24
32 Kako bismo usporedili stabilnosti mogućih međuprodukata oksidacije aminoazobenzena, proveli smo niz računa na SMD/M06-2X/6-311+G(2d,p) razini teorije. Da bi detaljnije istražili problem oksidacije, modelirali smo i varijante spojeva sa supstituentom X (X = CF 3, OCH 3 i C CH) u para- položaju azobenzena. Dobivene vrijednosti relativnih standardnih Gibbsovih energija prikazane su u Tablici 3. 25
33 Tablica 3. Relativne stabilnosti mogućih produkata oksidacije 4-aminoazobenzena Ime spoja ΔG rel / kcal/mol H CF 3 OCH 3 C CH aminoazoksi(2)benzen 0,20 0,00 0,11 0,00 aminoazoksi(3)benzen 0,00 0,60 0,00 0,43 Hidroksilaminoazobenzen 10,20 10,02 10,11 10,06 cis-hidroksilaminoazobenzen 20,33 hidroksilaminoazoksi(2)benzen 0,19 hidroksilaminoazoksi(3)benzen 0,00 Aminoazodioksibenzen 8,02 Dobiveni rezultati, odnosno relativne standardne Gibbsove energije pokazuju da se oksidacijom aminoazobenzena u slučaju termodinamičke kontrole dobiva aminoazoksibenzen, a ne hidroksilaminazobenzen. Taj rezultat sugerira da je oksidacija azo skupine u azoksi skupinu termodinamički povoljnija od oksidacije amino skupine u hidroksilaminsku, što je u skladu od poznatih eksperimentalnih podataka. 2 U drugom koraku preferencijalno će nastati hidroksilaminoazoksibenzen, a ne aminoazodioksibenzen. Termodinamički najpovoljniji reakcijski put prikazan je na Slici 6. Prema ovim rezultatima, za uspješnu sintezu nitrozoazobenzena trebalo bi odabrati oksidans, odnosno reducens koji bi stabilizirao prijelazno stanje te kinetički kontrolirao nastanak produkta. Za supstitente su uzete u obzir elektron-izvlačeće i elektron-donirajuće skupine, s pretpostavkom da bi neke od njih mogle usmjeriti sintezu putem koji će dovesti do ciljnog produkta. Kao što je vidljivo iz Tablice 3, utjecaj supstituenata značajno ne mijenja odnos energija različitih međuprodukata. 26
34 Slika 6. Termodinamički najstabilniji oksidacijski put 4-aminoazobenzena 27
35 5. ZAKLJUČAK Cilj ovog rada bio je pristup pripravi 4-nitrozoazobenzena. U skladu s dosadašnjim istraživanjima, sintezi takvog nitrozo spoja pristupilo se korištenjem oksidacijskih i redukcijskih metoda. 2 Prvi, oksidacijski pristup sintezi uključivao je oksidaciju komercijalno dostupnog 4-aminoazobenzena Oxone-om. Međutim, takav pristup nije dao željeni spoj, rezultirao je u nastanku nitro-, a ne nitrozo- derivata u širokom rasponu reakcijskih uvjeta. Redukcijom nitroazobenzena dobiven je hidroksilaminoazobenzen. Njegovom daljnjom oksidacijom dobiva se aminoazobenzen, a ne željeni nitrozoazobenzen. Prema tome, ciljni nitrozo spoj je vjerojatno nestabilni reakcijski međuprodukt u redoks nizu, koji se velikom brzinom raspada zbog čega ga nije bilo moguće izolirati. Da bi se razjasnila nemogućnost dobivanja nitrozo produkta oksidacijskim metodama pristupilo se računalnom pristupu. Korištenjem DFT metode, ispitana je bazičnost aminoazobenzena te relativna stabilnost i utjecaj supstituenata na moguće međuprodukte oksidacije. Izračunatom bazičnosti, na razini teorije SMD/M06-2X/6-311+G(2d,p) dobivena je pk b vrijednost β-dušikovog atoma u iznosu od 10,2, čime je potvrđeno istraživanje Rogersa da je bazičniji β-dušikov atom. 18 Drugi po bazičnosti je dušik amino skupine čija pk b vrijednost iznosi 11,5. Dakle, može se zaključiti da će se ti dušikovi atomi vjerojatnije protonirati u kiseloj otopini i na taj način onemogućiti oksidaciju. Dobivene vrijednosti energija mogućih međuprodukata oksidacije pokazale su kako u uvjetima termodinamičke kontrole iz aminoazobenzena prvo nastaje aminoazoksibenzen, zatim hidroksilaminoazoksibenzen i konačno hidroksilaminoazodioksibenzen. Takav rezultat sugerira kako je za dobivanje 4-nitrozoazobenzena potreban specifičan oksidans, odnosno reducens. 28
36 6. LITERATURNI IZVORI 1. V. Šimunić-Mežnarić, H. Vančik, O monomernim i dimernim oblicima nitrozo spojeva, Kem Ind. 54 (2005) H. Vančik, Aromatic C-nitroso Compounds, Springer, Dordrecht, New York, K. Nakamoto, R. E. Rundle, J. Am. Chem. Soc. 78 (1956) K. G. Orrell, D. Stephenson, T. Rault, Magn. Reson. Chem.27 (1989) D. A. Fletcher, B. G. Gowenlock, K. G. Orrell, V. Šik, Magn. Reson. Chem. 33 (1995) D. A. Fletcher, B. G. Gowenlock, K. G. Orrell, J. Chem. Soc. Perkin Trans. 2 (1998) D. A. Fletcher, B. G. Gowenlock, K. G. Orrell, V. Šik, D. E. Hibbs, M. B. Hursthouse, K. M. A. Malik, J. Chem. Soc., Perkin Trans. 2 (1996) B. G. Gowenlock, J. Trotman, J. Chem. Soc. (1955) M. L. Greer, H. Sarker, M. E. Mendicino, S. C. Blackstock, J. Am. Chem. Soc. 11 (1995) J. W. Wajer, J. de Boer, Recueil 91 (1972) G. Gowenlock, G. B. Richter-Addo, Chem Rev. 104 (2004) S. Tollari, M. Cuscela, F. Porta, J. Chem. Soc. Chem. Commun. (1993) Fieser and Fieser s Reagents for Organic Synthesis, J. Wiley & Sons, New York, 4 (1984) W. W. Zajac Jr., M. G. Darcy, A. P. Subong, J. H. Buzby, Tetrahedron Lett. 30 (1989) E. J. Corey, A. W. Gross, Org. Synth. 65 (1987) B. S. Furniss, A. J. Hannaford, V. Rogers, P. W. G. Smith, A. R. Tatchell, Vogel s Textbook of Practical Organic Chemistry, 4th. ed., Longman, London, New York (1978) H. M. Dhammika Bandara, Shawn C. Burdette, Chem. Soc. Rev. 41 (2012) M. T. Rogers, T. W. Campbell, R. W. Maatman, J. Am. Chem. Soc. 73 (1951) E. Sawicki, J. Org. Chem. 22 (1957) W. Lüttke, P. N. Skancke, M. Traetteberg, Theor. Chim. Acta 87 (1994) V. Stepanić, G. Baranović, V. Smrečki, J. Mol. Struct. 569 (2001) T. Nagele, R. Hoche, W. Zinth, J. Wachtveitl, Chem. Phys. Lett. 272 (1997) E. Pretsch, J. Seibl, W. Simon, T. Clerc, Tablice za određivanje strukture organskih spojeva spektroskopskim metodama, SKTH/ Kemija u industriji, Zagreb, 1982, 24. B. G. Gowenlock, M. Cameron, A. S. F. Boyd, B. M. Al-Tahou, P. McKenna, Can. J. Chem. 72 (1994) K. M. Tait, J. A. Parkinson, S. P. Bates, J. Photochem. Photobiol.A. Chem. 154 (2003) H. Dürr, Angew. Chem. Int. Ed. Engl. 28 (1989) H. Dürr, Pure & Appl. Chem. 62 (1990)
37 28. H. Vančik, V. Šimunić-Mežnarić, I. Čaleta, E. Meštrović, S. Milovac, K. Mlinarić- Majerski, J. Veljković, J. Phys. Chem. B. 106 (2002) S. Milovac, V. Šimunić-Mežnarić, H. Vančik, A. Višnjevac, B. Kojić-Prodić, Acta Cryst. E57 (2001) L. Bluhm, J. Weinstein, Nature, 215 (1967) G. M. J. Schmidt, Solid State Photochemistry, D. Ginsburg (Ed.) Verlag Chemie, Weinheim, New York, M. Irie, T. Lifka, S. Kobatake, N. Kato, J. Am. Chem. Soc. 122 (2000) H. G. O. Becker, H. Böttcher, F. Dietz, D. Rehorek, G. Roewer, K. Schiller, H. J. Timpe, Einführung in die Photochemie, Deutscher Verlag der Wissenschaft: Berlin, 1991, J. W. Wajer, J. de Boer, Recueil 91 (1972) R. Lovrien, P. Pesheck, W. Tisel, J. Am. Chem. Soc. 96 (1974) P. Balaž, Mechanochemistry in Nanoscience and Minerals Engineering, Springer- Verlag, Berlin Heidelberg, V. A. Marenich, J. C. Cramer, G. D. Truhlar, J. Phys. Chem. B 113 (2009) Gaussian 09, Revision D.01, M. J. Frisch, G. W. Trucks, H. B. Schlegel, G. E. 39. S. Grimme, S. Ehrlich, L. Goerig, J. Comp. Chem. 32 (2011) Y. Zhao, G. D. Truhlar, Theor. Chem. Acc. 120 (2008) Christopher. J. Cramer, Essential of Computational of Chemistry Theories and Models, Second edition (2004.) 42. Scuseria, M. A. Robb, J. R. Cheeseman, G. Scalmani, V. Barone, B. Mennucci, G. A. Petersson, H. Nakatsuji, M. Caricato, X. Li, H. P. Hratchian, A. F. Izmaylov, J. Bloino, G. Zheng, J. L. Sonnenberg, M. Hada, M. Ehara, K. Toyota, R. Fukuda, J. Hasegawa, M. Ishida, T. Nakajima, Y. Honda, O. Kitao, H. Nakai, T. Vreven, J. A. Montgomery, Jr., J. E. Peralta, F. Ogliaro, M. Bearpark, J. J. Heyd, E. Brothers, K. N. Kudin, V. N. Staroverov, R. Kobayashi, J. Normand, K. Raghavachari, A. Rendell, J. C. Burant, S. S. Iyengar, J. Tomasi, M. Cossi, N. Rega, J. M. Millam, M. Klene, J. E. Knox, J. B. Cross, V. Bakken, C. Adamo, J. Jaramillo, R. Gomperts, R. E. Stratmann, O. Yazyev, A. J. Austin, R. Cammi, C. Pomelli, J. W. Ochterski, R. L. Martin, K. Morokuma, V. G. Zakrzewski, G. A. Voth, P. Salvador, J. J. Dannenberg, S. Dapprich, A. D. Daniels, Ö. Farkas, J. B. Foresman, J. V. Ortiz, J. Cioslowski, and D. J. Fox, Gaussian, Inc., Wallingford CT, M. Namazian, F. Kalantary-Fotooh, R. M. Noorbala, J. D. Searles, L. M. Coote, J. Mol. Str. THEOCHEM 758 (2006) A. Defoin, Synthesis (2004)
38 7. DODATAK 7.1. IR spektri Slika IR spektar 4-nitroazobenzena dobivenog oksidacijom 4-aminoazobenzena. Slika IR spektar 4-aminoazobenzena dobivenog redukcijom 4-nitroazobenzena. VIII
39 7.2. NMR spektri Slika H NMR spektar 4-nitroazobenzena sintetiziranog oksidacijom 4-aminoazobenzena oksonom. Slika C NMR spektar 4-nitroazobenzena sintetiziranog oksidacijom 4-aminoazobenzena oksonom. IX
40 Slika H NMR spektar 4-aminoazobenzena sintetiziranog redukcijom 4-nitroazobenzena MS spektar Slika 7.3. Spektar masa nitroazobenzena dobiven ionizacijom elektronima uz kvadrupolnu stupicu za ione. X
41 8. ŽIVOTOPIS Rođena sam 29. kolovoza godine u Zagrebu. Osnovnu školu Mate Lovraka završila sam godine s izvrsnim uspjehom. Nakon završene opće XII. Gimnazije u Zagrebu, s izvrsnim uspjehom, te oslobođenja od polaganja mature upisala sam Prirodoslovnomatematički fakultet u Zagrebu. Akademski stupanj Prvostupnice kemije stekla sam godine i iste godine upisala diplomski studij kemije na Prirodoslovno-matematičkom fakultetu u Zagrebu, istraživački smjer, grane organska i analitička kemija. Na istom fakultetu godine sam upisala nastavnički smjer kemije. Ove godine sudjelujem u znanstveno popularnoj manifestaciji pod nazivom Otvoreni dan kemije, gdje se na zanimljiv način prezentira kemija za učenike osnovnih i srednjih škola. XI
Electronic Supplementary Information (ESI) for Chem. Commun.
 page S1 Electronic Supplementary Information (ESI) for Chem. Commun. Nitric oxide coupling mediated by iron porphyrins: the N-N bond formation step is facilitated by electrons and a proton Jun Yi, Brian
page S1 Electronic Supplementary Information (ESI) for Chem. Commun. Nitric oxide coupling mediated by iron porphyrins: the N-N bond formation step is facilitated by electrons and a proton Jun Yi, Brian
Group 13 BN dehydrocoupling reagents, similar to transition metal catalysts but with unique reactivity. Part A: NMR Studies
 Part A: NMR Studies ESI 1 11 B NMR spectrum of the 2:1 reaction of i Pr 2 NHBH 3 with Al(NMe 2 ) 3 in d 6 -benzene 24 h later 11 B NMR ESI 2 11 B NMR spectrum of the reaction of t BuNH 2 BH 3 with Al(NMe
Part A: NMR Studies ESI 1 11 B NMR spectrum of the 2:1 reaction of i Pr 2 NHBH 3 with Al(NMe 2 ) 3 in d 6 -benzene 24 h later 11 B NMR ESI 2 11 B NMR spectrum of the reaction of t BuNH 2 BH 3 with Al(NMe
A Computational Model for the Dimerization of Allene: Supporting Information
 A Computational Model for the Dimerization of Allene: Supporting Information Sarah L. Skraba and Richard P. Johnson* Department of Chemistry University of New Hampshire Durham, NH 03824 Corresponding Author:
A Computational Model for the Dimerization of Allene: Supporting Information Sarah L. Skraba and Richard P. Johnson* Department of Chemistry University of New Hampshire Durham, NH 03824 Corresponding Author:
SUPPORTING INFORMATION. Ammonia-Borane Dehydrogenation Promoted by a Pincer-Square- Planar Rhodium(I)-Monohydride: A Stepwise Hydrogen Transfer
 S 1 SUPPORTING INFORMATION Ammonia-Borane Dehydrogenation Promoted by a Pincer-Square- Planar Rhodium(I)-Monohydride: A Stepwise Hydrogen Transfer from the Substrate to the Catalyst Miguel A. Esteruelas,*
S 1 SUPPORTING INFORMATION Ammonia-Borane Dehydrogenation Promoted by a Pincer-Square- Planar Rhodium(I)-Monohydride: A Stepwise Hydrogen Transfer from the Substrate to the Catalyst Miguel A. Esteruelas,*
Supporting Information. 4-Pyridylnitrene and 2-pyrazinylcarbene
 Supporting Information for 4-Pyridylnitrene and 2-pyrazinylcarbene Curt Wentrup*, Ales Reisinger and David Kvaskoff Address: School of Chemistry and Molecular Biosciences, The University of Queensland,
Supporting Information for 4-Pyridylnitrene and 2-pyrazinylcarbene Curt Wentrup*, Ales Reisinger and David Kvaskoff Address: School of Chemistry and Molecular Biosciences, The University of Queensland,
Supporting Information
 Theoretical examination of competitive -radical-induced cleavages of N-C and C -C bonds of peptides Wai-Kit Tang, Chun-Ping Leong, Qiang Hao, Chi-Kit Siu* Department of Biology and Chemistry, City University
Theoretical examination of competitive -radical-induced cleavages of N-C and C -C bonds of peptides Wai-Kit Tang, Chun-Ping Leong, Qiang Hao, Chi-Kit Siu* Department of Biology and Chemistry, City University
Supporting Information For. metal-free methods for preparation of 2-acylbenzothiazoles and. dialkyl benzothiazole-2-yl phosphonates
 Supporting Information For Peroxide as switch of dialkyl H-phosphonate: two mild and metal-free methods for preparation of 2-acylbenzothiazoles and dialkyl benzothiazole-2-yl phosphonates Xiao-Lan Chen,*,
Supporting Information For Peroxide as switch of dialkyl H-phosphonate: two mild and metal-free methods for preparation of 2-acylbenzothiazoles and dialkyl benzothiazole-2-yl phosphonates Xiao-Lan Chen,*,
Mechanism of Hydrogen Evolution in Cu(bztpen)-Catalysed Water Reduction: A DFT Study
 Electronic Supplementary Material (ESI) for Dalton Transactions. This journal is The Royal Society of Chemistry 2015 Supporting Information to Mechanism of Hydrogen Evolution in Cu(bztpen)-Catalysed Water
Electronic Supplementary Material (ESI) for Dalton Transactions. This journal is The Royal Society of Chemistry 2015 Supporting Information to Mechanism of Hydrogen Evolution in Cu(bztpen)-Catalysed Water
Supporting Information
 Rich coordination chemistry of π-acceptor dibenzoarsole ligands Arvind Kumar Gupta, 1 Sunisa Akkarasamiyo, 2 Andreas Orthaber*,1 1 Molecular Inorganic Chemistry, Department of Chemistry, Ångström Laboratories,
Rich coordination chemistry of π-acceptor dibenzoarsole ligands Arvind Kumar Gupta, 1 Sunisa Akkarasamiyo, 2 Andreas Orthaber*,1 1 Molecular Inorganic Chemistry, Department of Chemistry, Ångström Laboratories,
Supporting Information. {RuNO} 6 vs. Co-Ligand Oxidation: Two Non-Innocent Groups in One Ruthenium Nitrosyl Complex
 Electronic Supplementary Material (ESI) for Dalton Transactions. This journal is The Royal Society of Chemistry 2014 Supporting Information {RuNO} 6 vs. Co-Ligand Oxidation: Two Non-Innocent Groups in
Electronic Supplementary Material (ESI) for Dalton Transactions. This journal is The Royal Society of Chemistry 2014 Supporting Information {RuNO} 6 vs. Co-Ligand Oxidation: Two Non-Innocent Groups in
Two-Dimensional Carbon Compounds Derived from Graphyne with Chemical Properties Superior to Those of Graphene
 Supplementary Information Two-Dimensional Carbon Compounds Derived from Graphyne with Chemical Properties Superior to Those of Graphene Jia-Jia Zheng, 1,2 Xiang Zhao, 1* Yuliang Zhao, 2 and Xingfa Gao
Supplementary Information Two-Dimensional Carbon Compounds Derived from Graphyne with Chemical Properties Superior to Those of Graphene Jia-Jia Zheng, 1,2 Xiang Zhao, 1* Yuliang Zhao, 2 and Xingfa Gao
Supporting Information. O-Acetyl Side-chains in Saccharides: NMR J-Couplings and Statistical Models for Acetate Ester Conformational Analysis
 Supporting Information -Acetyl Side-chains in Saccharides: NMR J-Couplings and Statistical Models for Acetate Ester Conformational Analysis Toby Turney, Qingfeng Pan, Luke Sernau, Ian Carmichael, Wenhui
Supporting Information -Acetyl Side-chains in Saccharides: NMR J-Couplings and Statistical Models for Acetate Ester Conformational Analysis Toby Turney, Qingfeng Pan, Luke Sernau, Ian Carmichael, Wenhui
CICECO, Departamento de Química, Universidade de Aveiro, Aveiro, Portugal
 Evidence for the Interactions Occurring between Ionic Liquids and Tetraethylene Glycol in Binary Mixtures and Aqueous Biphasic Systems Luciana I. N. Tomé, Jorge F. B. Pereira,, Robin D. Rogers, Mara G.
Evidence for the Interactions Occurring between Ionic Liquids and Tetraethylene Glycol in Binary Mixtures and Aqueous Biphasic Systems Luciana I. N. Tomé, Jorge F. B. Pereira,, Robin D. Rogers, Mara G.
Supplementary Information:
 Electronic Supplementary Material (ESI) for Dalton Transactions. This journal is The Royal Society of Chemistry 2016 Supplementary Information: Coordination and Insertion of Alkenes and Alkynes in Au III
Electronic Supplementary Material (ESI) for Dalton Transactions. This journal is The Royal Society of Chemistry 2016 Supplementary Information: Coordination and Insertion of Alkenes and Alkynes in Au III
Supporting Information. Detection of Leucine Aminopeptidase Activity in Serum Using. Surface-Enhanced Raman Spectroscopy
 Electronic Supplementary Material (ESI) for Analyst. This journal is The Royal Society of Chemistry 2018 Supporting Information Detection of Leucine Aminopeptidase Activity in Serum Using Surface-Enhanced
Electronic Supplementary Material (ESI) for Analyst. This journal is The Royal Society of Chemistry 2018 Supporting Information Detection of Leucine Aminopeptidase Activity in Serum Using Surface-Enhanced
SUPPLEMENTARY INFORMATION
 Electronic Supplementary Material (ESI) for Dalton Transactions. This journal is The Royal Society of Chemistry 2015 Novel B(Ar') 2 (Ar'') hetero-tri(aryl)boranes: a systematic study of Lewis acidity Robin
Electronic Supplementary Material (ESI) for Dalton Transactions. This journal is The Royal Society of Chemistry 2015 Novel B(Ar') 2 (Ar'') hetero-tri(aryl)boranes: a systematic study of Lewis acidity Robin
The Activation of Carboxylic Acids via Self Assembly Asymmetric Organocatalysis: A Combined Experimental and Computational Investigation
 The Activation of Carboxylic Acids via Self Assembly Asymmetric Organocatalysis: A Combined Experimental and Computational Investigation Mattia Riccardo Monaco, Daniele Fazzi, Nobuya Tsuji, Markus Leutzsch,
The Activation of Carboxylic Acids via Self Assembly Asymmetric Organocatalysis: A Combined Experimental and Computational Investigation Mattia Riccardo Monaco, Daniele Fazzi, Nobuya Tsuji, Markus Leutzsch,
Experimental Evidence for Non-Canonical Thymine Cation Radicals in the Gas Phase
 Supporting Information for Experimental Evidence for Non-Canonical Thymine Cation Radicals in the Gas Phase Andy Dang, Huong T. H. Nguyen, Heather Ruiz, Elettra Piacentino,Victor Ryzhov *, František Tureček
Supporting Information for Experimental Evidence for Non-Canonical Thymine Cation Radicals in the Gas Phase Andy Dang, Huong T. H. Nguyen, Heather Ruiz, Elettra Piacentino,Victor Ryzhov *, František Tureček
Supporting Information
 Quantum Chemistry Study of U(VI), Np(V) and Pu(IV,VI) Complexes with Preorganized Tetradentate Phenanthroline Amide Ligands Cheng-Liang Xiao, Qun-Yan Wu, Cong-Zhi Wang, Yu-Liang Zhao, Zhi-Fang Chai, *
Quantum Chemistry Study of U(VI), Np(V) and Pu(IV,VI) Complexes with Preorganized Tetradentate Phenanthroline Amide Ligands Cheng-Liang Xiao, Qun-Yan Wu, Cong-Zhi Wang, Yu-Liang Zhao, Zhi-Fang Chai, *
Supporting Information
 Supporting Information Z-Selective Ethenolysis With a Ruthenium Metathesis Catalyst: Experiment and Theory Hiroshi Miyazaki,, Myles B. Herbert,, Peng Liu, Xiaofei Dong, Xiufang Xu,,# Benjamin K. Keitz,
Supporting Information Z-Selective Ethenolysis With a Ruthenium Metathesis Catalyst: Experiment and Theory Hiroshi Miyazaki,, Myles B. Herbert,, Peng Liu, Xiaofei Dong, Xiufang Xu,,# Benjamin K. Keitz,
Non-Radiative Decay Paths in Rhodamines: New. Theoretical Insights
 Electronic Supplementary Material (ESI) for Physical Chemistry Chemical Physics. This journal is the Owner Societies 2014 Non-Radiative Decay Paths in Rhodamines: New Theoretical Insights Marika Savarese,
Electronic Supplementary Material (ESI) for Physical Chemistry Chemical Physics. This journal is the Owner Societies 2014 Non-Radiative Decay Paths in Rhodamines: New Theoretical Insights Marika Savarese,
Supporting Information Computational Part
 Supporting Information Computational Part The Cinchona Primary Amine-Catalyzed Asymmetric Epoxidation and Hydroperoxidation of, -Unsaturated Carbonyl Compounds with Hydrogen Peroxide Olga Lifchits, Manuel
Supporting Information Computational Part The Cinchona Primary Amine-Catalyzed Asymmetric Epoxidation and Hydroperoxidation of, -Unsaturated Carbonyl Compounds with Hydrogen Peroxide Olga Lifchits, Manuel
Scalable synthesis of quaterrylene: solution-phase
 PT2 PT2 P 2PT......... Electronic Supplementary Information For Scalable synthesis of quaterrylene: solution-phase 1 PH NMR spectroscopy of its oxidative dication Rajesh Thamatam, Sarah L. Skraba and Richard
PT2 PT2 P 2PT......... Electronic Supplementary Information For Scalable synthesis of quaterrylene: solution-phase 1 PH NMR spectroscopy of its oxidative dication Rajesh Thamatam, Sarah L. Skraba and Richard
ELECTRONIC SUPPLEMENTARY INFORMATION
 Electronic Supplementary Material (ESI) for Physical Chemistry Chemical Physics. This journal is the Owner Societies 2017 S-1 ELECTRONIC SUPPLEMENTARY INFORMATION OCT. 1, 2017 Combined Quantum Mechanical
Electronic Supplementary Material (ESI) for Physical Chemistry Chemical Physics. This journal is the Owner Societies 2017 S-1 ELECTRONIC SUPPLEMENTARY INFORMATION OCT. 1, 2017 Combined Quantum Mechanical
SUPPORTING INFORMATION
 SUPPORTING INFORMATION Revisiting the long-range Perlin effect in a conformationally constrained Oxocane Kahlil S. Salome and Cláudio F. Tormena* Institute of Chemistry, University of Campinas - UNICAMP
SUPPORTING INFORMATION Revisiting the long-range Perlin effect in a conformationally constrained Oxocane Kahlil S. Salome and Cláudio F. Tormena* Institute of Chemistry, University of Campinas - UNICAMP
Supplementary Information
 Supplementary Information Enhancing the Double Exchange Interaction in Mixed Valence {V III -V II } Pair: A Theoretical Perspective Soumen Ghosh, Saurabh Kumar Singh and Gopalan Rajaraman* a Computational
Supplementary Information Enhancing the Double Exchange Interaction in Mixed Valence {V III -V II } Pair: A Theoretical Perspective Soumen Ghosh, Saurabh Kumar Singh and Gopalan Rajaraman* a Computational
3,4-Ethylenedioxythiophene (EDOT) and 3,4- Ethylenedioxyselenophene (EDOS): Synthesis and Reactivity of
 Supporting Information 3,4-Ethylenedioxythiophene (EDOT) and 3,4- Ethylenedioxyselenophene (EDOS): Synthesis and Reactivity of C α -Si Bond Soumyajit Das, Pradip Kumar Dutta, Snigdha Panda, Sanjio S. Zade*
Supporting Information 3,4-Ethylenedioxythiophene (EDOT) and 3,4- Ethylenedioxyselenophene (EDOS): Synthesis and Reactivity of C α -Si Bond Soumyajit Das, Pradip Kumar Dutta, Snigdha Panda, Sanjio S. Zade*
Nucleophilicity Evaluation for Primary and Secondary Amines
 Nucleophilicity Evaluation for Primary and Secondary Amines MADIAN RAFAILA, MIHAI MEDELEANU*, CORNELIU MIRCEA DAVIDESCU Politehnica University of Timiºoara, Faculty of Industrial Chemistry and Environmental
Nucleophilicity Evaluation for Primary and Secondary Amines MADIAN RAFAILA, MIHAI MEDELEANU*, CORNELIU MIRCEA DAVIDESCU Politehnica University of Timiºoara, Faculty of Industrial Chemistry and Environmental
Elucidating the structure of light absorbing styrene. carbocation species formed within zeolites SUPPORTING INFORMATION
 Electronic Supplementary Material (ESI) for Physical Chemistry Chemical Physics. This journal is the Owner Societies 2017 Elucidating the structure of light absorbing styrene carbocation species formed
Electronic Supplementary Material (ESI) for Physical Chemistry Chemical Physics. This journal is the Owner Societies 2017 Elucidating the structure of light absorbing styrene carbocation species formed
Out-Basicity of 1,8-bis(dimethylamino)naphthalene: The experimental and theoretical challenge
 S1 Supplementary information for Out-Basicity of 1,8-bis(dimethylamino)naphthalene: The experimental and theoretical challenge Valery A. Ozeryanskii, a Alexander F. Pozharskii,,a Alexander S. Antonov a
S1 Supplementary information for Out-Basicity of 1,8-bis(dimethylamino)naphthalene: The experimental and theoretical challenge Valery A. Ozeryanskii, a Alexander F. Pozharskii,,a Alexander S. Antonov a
BINOPtimal: A Web Tool for Optimal Chiral Phosphoric Acid Catalyst Selection
 Electronic Supplementary Material (ESI) for ChemComm. This journal is The Royal Society of Chemistry 2019 BINOPtimal: A Web Tool for Optimal Chiral Phosphoric Acid Catalyst Selection Jolene P. Reid, Kristaps
Electronic Supplementary Material (ESI) for ChemComm. This journal is The Royal Society of Chemistry 2019 BINOPtimal: A Web Tool for Optimal Chiral Phosphoric Acid Catalyst Selection Jolene P. Reid, Kristaps
Driving forces for the self-assembly of graphene oxide on organic monolayers
 Electronic Supplementary Material (ESI) for Nanoscale. This journal is The Royal Society of Chemistry 2014 Supporting Information Driving forces for the self-assembly of graphene oxide on organic monolayers
Electronic Supplementary Material (ESI) for Nanoscale. This journal is The Royal Society of Chemistry 2014 Supporting Information Driving forces for the self-assembly of graphene oxide on organic monolayers
Supporting information
 Supporting information Metal free Markovnikov type alkyne hydration under mild conditions Wenbo Liu, Haining Wang and Chao-Jun Li * Department of Chemistry and FQRNT Center for Green Chemistry and Catalysis,
Supporting information Metal free Markovnikov type alkyne hydration under mild conditions Wenbo Liu, Haining Wang and Chao-Jun Li * Department of Chemistry and FQRNT Center for Green Chemistry and Catalysis,
Electronic Supplementary Information. Electron Mobility for All-Polymer Solar Cells
 Electronic Supplementary Material (ESI) for Materials Chemistry Frontiers. This journal is the Partner Organisations 2018 Electronic Supplementary Information for Double B N Bridged Bipyridine-Containing
Electronic Supplementary Material (ESI) for Materials Chemistry Frontiers. This journal is the Partner Organisations 2018 Electronic Supplementary Information for Double B N Bridged Bipyridine-Containing
Table S1: DFT computed energies of high spin (HS) and broken symmetry (BS) state, <S 2 > values for different radical systems. HS BS1 BS2 BS3 < S 2 >
 Computational details: The magnetic exchange interaction between the Gd(III) centers in the non-radical bridged complex has been evaluated using the following Hamiltonian relation, = 2J J represents the
Computational details: The magnetic exchange interaction between the Gd(III) centers in the non-radical bridged complex has been evaluated using the following Hamiltonian relation, = 2J J represents the
Supplementary information
 Supplementary information doi: 10.1038/nchem.287 A Potential Energy Surface Bifurcation in Terpene Biosynthesis Young J. Hong and Dean J. Tantillo* Department of Chemistry, University of California, Davis,
Supplementary information doi: 10.1038/nchem.287 A Potential Energy Surface Bifurcation in Terpene Biosynthesis Young J. Hong and Dean J. Tantillo* Department of Chemistry, University of California, Davis,
A mechanistic study supports a two-step mechanism for peptide bond formation on the ribosome
 s1 Electronic Supplementary Information A mechanistic study supports a two-step mechanism for peptide bond formation on the ribosome Byung Jin Byun and Young Kee Kang* Department of Chemistry, Chungbuk
s1 Electronic Supplementary Information A mechanistic study supports a two-step mechanism for peptide bond formation on the ribosome Byung Jin Byun and Young Kee Kang* Department of Chemistry, Chungbuk
Cationic Polycyclization of Ynamides: Building up Molecular Complexity
 Electronic Supplementary Material (ESI) for Organic & Biomolecular Chemistry. This journal is The Royal Society of Chemistry 2017 Supporting Information Cationic Polycyclization of Ynamides: Building up
Electronic Supplementary Material (ESI) for Organic & Biomolecular Chemistry. This journal is The Royal Society of Chemistry 2017 Supporting Information Cationic Polycyclization of Ynamides: Building up
INTERNATIONAL JOURNAL OF RESEARCH IN COMPUTER APPLICATIONS AND ROBOTICS ISSN
 INTERNATIONAL JOURNAL OF RESEARCH IN COMPUTER APPLICATIONS AND ROBOTICS ISSN 2320-7345 THEORETICAL APPROACH TO THE EVALUATION OF ACTIVATION ENERGIES I. Hammoudan 1, D. Riffi Temsamani 2, 1 Imad_2005_05@hotmail.com
INTERNATIONAL JOURNAL OF RESEARCH IN COMPUTER APPLICATIONS AND ROBOTICS ISSN 2320-7345 THEORETICAL APPROACH TO THE EVALUATION OF ACTIVATION ENERGIES I. Hammoudan 1, D. Riffi Temsamani 2, 1 Imad_2005_05@hotmail.com
Supplementary Material: 2D-IR Spectroscopy of an AHA Labelled Photoswitchable PDZ2 Domain
 Supplementary Material: 2D-IR Spectroscopy of an AHA Labelled Photoswitchable PDZ2 Domain Brigitte Stucki-Buchli, Philip Johnson, Olga Bozovic, Claudio Zanobini, Klemens Koziol, Peter Hamm Department of
Supplementary Material: 2D-IR Spectroscopy of an AHA Labelled Photoswitchable PDZ2 Domain Brigitte Stucki-Buchli, Philip Johnson, Olga Bozovic, Claudio Zanobini, Klemens Koziol, Peter Hamm Department of
Detailed Syntheses. K 5H[Co II W 12O 40] 15H 2O (1). The synthesis was adapted from published methods. [1] Sodium tungstate
![Detailed Syntheses. K 5H[Co II W 12O 40] 15H 2O (1). The synthesis was adapted from published methods. [1] Sodium tungstate Detailed Syntheses. K 5H[Co II W 12O 40] 15H 2O (1). The synthesis was adapted from published methods. [1] Sodium tungstate](/thumbs/93/114178575.jpg) Detailed Syntheses K 5H[Co II W 12O 40] 15H 2O (1). The synthesis was adapted from published methods. [1] Sodium tungstate dihydrate (19.8 g, 60 mmol) was dissolved with stirring in 40 ml of deionized
Detailed Syntheses K 5H[Co II W 12O 40] 15H 2O (1). The synthesis was adapted from published methods. [1] Sodium tungstate dihydrate (19.8 g, 60 mmol) was dissolved with stirring in 40 ml of deionized
A dominant homolytic O-Cl bond cleavage with low-spin triplet-state Fe(IV)=O formed is revealed in the mechanism of heme-dependent chlorite dismutase
 Supplementary Information to: A dominant homolytic O-Cl bond cleavage with low-spin triplet-state Fe(IV)=O formed is revealed in the mechanism of heme-dependent chlorite dismutase Shuo Sun, Ze-Sheng Li,
Supplementary Information to: A dominant homolytic O-Cl bond cleavage with low-spin triplet-state Fe(IV)=O formed is revealed in the mechanism of heme-dependent chlorite dismutase Shuo Sun, Ze-Sheng Li,
Department of Chemistry, School of life Science and Technology, Jinan University, Guangzhou , China b
 Electronic Supplementary Material (ESI) for ChemComm. This journal is The Royal Society of Chemistry 2015 Electronic Supplementary Information for A Br substituted phenanthroimidazole derivative with aggregation
Electronic Supplementary Material (ESI) for ChemComm. This journal is The Royal Society of Chemistry 2015 Electronic Supplementary Information for A Br substituted phenanthroimidazole derivative with aggregation
Supporting Information
 Supporting Information Rhodium-Catalyzed Synthesis of Imines and Esters from Benzyl Alcohols and Nitroarenes: Change in Catalyst Reactivity Depending on the Presence or Absence of the Phosphine Ligand
Supporting Information Rhodium-Catalyzed Synthesis of Imines and Esters from Benzyl Alcohols and Nitroarenes: Change in Catalyst Reactivity Depending on the Presence or Absence of the Phosphine Ligand
Electrochemical Reduction of Aqueous Imidazolium on Pt (111) by Proton Coupled Electron Transfer
 Supporting Information for Electrochemical Reduction of Aqueous Imidazolium on Pt (111) by Proton Coupled Electron Transfer Kuo Liao 1, Mikhail Askerka 2, Elizabeth L. Zeitler 1, Andrew B. Bocarsly 1*
Supporting Information for Electrochemical Reduction of Aqueous Imidazolium on Pt (111) by Proton Coupled Electron Transfer Kuo Liao 1, Mikhail Askerka 2, Elizabeth L. Zeitler 1, Andrew B. Bocarsly 1*
Interfacial Hydration Dynamics in Cationic Micelles Using 2D-IR and NMR
 Supplementary Information Interfacial Hydration Dynamics in Cationic Micelles Using 2D-IR and NMR Ved Prakash Roy and Kevin J. Kubarych* Department of Chemistry, University of Michigan, 930 N. University
Supplementary Information Interfacial Hydration Dynamics in Cationic Micelles Using 2D-IR and NMR Ved Prakash Roy and Kevin J. Kubarych* Department of Chemistry, University of Michigan, 930 N. University
Electronic Supporting Information
 Electronic Supplementary Material (ESI) for Chemical Science. This journal is The Royal Society of Chemistry 2015 Electronic Supporting Information Materials and methods 1,2-Bis[2,5-dimethyl(3-thienyl)]ethane-1,2-dione
Electronic Supplementary Material (ESI) for Chemical Science. This journal is The Royal Society of Chemistry 2015 Electronic Supporting Information Materials and methods 1,2-Bis[2,5-dimethyl(3-thienyl)]ethane-1,2-dione
Supporting Information for. Acceptor-Type Hydroxide Graphite Intercalation Compounds. Electrochemically Formed in High Ionic Strength Solutions
 Electronic Supplementary Material (ESI) for ChemComm. This journal is The Royal Society of Chemistry 2017 Supporting Information for Acceptor-Type Hydroxide Graphite Intercalation Compounds Electrochemically
Electronic Supplementary Material (ESI) for ChemComm. This journal is The Royal Society of Chemistry 2017 Supporting Information for Acceptor-Type Hydroxide Graphite Intercalation Compounds Electrochemically
DFT and TDDFT calculation of lead chalcogenide clusters up to (PbX) 32
 DFT and TDDFT calculation of lead chalcogenide clusters up to (PbX) 32 V. S. Gurin Research Institute for Physical Chemical Problems, Belarusian State University, Leningradskaya 14, 220006, Minsk, Belarus
DFT and TDDFT calculation of lead chalcogenide clusters up to (PbX) 32 V. S. Gurin Research Institute for Physical Chemical Problems, Belarusian State University, Leningradskaya 14, 220006, Minsk, Belarus
SUPPLEMENTARY MATERIAL. Nitrogen Containing Ionic Liquids: Biodegradation Studies and
 S1 10.1071/CH14499_AC CSIRO 2015 Australian Journal of Chemistry 2015, 68 (6), 849-857 SUPPLEMENTARY MATERIAL Nitrogen Containing Ionic Liquids: Biodegradation Studies and Utility in Base Mediated Reactions
S1 10.1071/CH14499_AC CSIRO 2015 Australian Journal of Chemistry 2015, 68 (6), 849-857 SUPPLEMENTARY MATERIAL Nitrogen Containing Ionic Liquids: Biodegradation Studies and Utility in Base Mediated Reactions
Electronic relaxation dynamics of PCDA PDA studied by transient absorption spectroscopy
 Electronic Supplementary Material (ESI) for Physical Chemistry Chemical Physics. his journal is the Owner Societies 06 Electronic Supplementary Information for Electronic relaxation dynamics of PCDA PDA
Electronic Supplementary Material (ESI) for Physical Chemistry Chemical Physics. his journal is the Owner Societies 06 Electronic Supplementary Information for Electronic relaxation dynamics of PCDA PDA
Asymmetric Redox-Annulation of Cyclic Amines. Supporting Information
 Asymmetric Redox-Annulation of Cyclic Amines YoungKu Kang, Weijie Chen, Martin Breugst,, * and Daniel Seidel, * Department of Chemistry and Chemical Biology, Rutgers, The State University of New Jersey,
Asymmetric Redox-Annulation of Cyclic Amines YoungKu Kang, Weijie Chen, Martin Breugst,, * and Daniel Seidel, * Department of Chemistry and Chemical Biology, Rutgers, The State University of New Jersey,
SUPPORTING INFORMATION. Mechanistic Analysis of Water Oxidation Catalyzed by Mononuclear Copper in Aqueous Bicarbonate Solutions
 Electronic Supplementary Material (ESI) for Catalysis Science & Technology. This journal is The Royal Society of Chemistry 2014 draft of April 10, 2014 SUPPRTING INFRMATIN Mechanistic Analysis of Water
Electronic Supplementary Material (ESI) for Catalysis Science & Technology. This journal is The Royal Society of Chemistry 2014 draft of April 10, 2014 SUPPRTING INFRMATIN Mechanistic Analysis of Water
Supporting Information. Reactive Simulations-based Model for the Chemistry behind Condensed Phase Ignition in RDX crystals from Hot Spots
 Electronic Supplementary Material (ESI) for Physical Chemistry Chemical Physics. This journal is the Owner Societies 2015 Supporting Information Reactive Simulations-based Model for the Chemistry behind
Electronic Supplementary Material (ESI) for Physical Chemistry Chemical Physics. This journal is the Owner Societies 2015 Supporting Information Reactive Simulations-based Model for the Chemistry behind
Supporting Information
 Supporting Information Formate to Oxalate: A Crucial Step for the Conversion of Carbon Dioxide into Multi-carbon Compounds Prasad S. Lakkaraju,* [b] Mikhail Askerka, [a] Heidie Beyer, [b] Charles T. Ryan,
Supporting Information Formate to Oxalate: A Crucial Step for the Conversion of Carbon Dioxide into Multi-carbon Compounds Prasad S. Lakkaraju,* [b] Mikhail Askerka, [a] Heidie Beyer, [b] Charles T. Ryan,
Supporting Information
 Supporting Information Wiley-VCH 2007 69451 Weinheim, Germany Aluminum Siting in Silicon-rich Zeolite Frameworks. A Combined High Resolution 27 Al NMR and QM/MM Study of ZSM-5 Stepan Sklenak,* Jiří Dědeček,
Supporting Information Wiley-VCH 2007 69451 Weinheim, Germany Aluminum Siting in Silicon-rich Zeolite Frameworks. A Combined High Resolution 27 Al NMR and QM/MM Study of ZSM-5 Stepan Sklenak,* Jiří Dědeček,
Supporting Information
 Electronic Supplementary Material (ESI) for Nanoscale. This journal is The Royal Society of Chemistry 2018 Supporting Information A self-powered porous ZnS/PVDF-HFP mechanoluminescent composite film that
Electronic Supplementary Material (ESI) for Nanoscale. This journal is The Royal Society of Chemistry 2018 Supporting Information A self-powered porous ZnS/PVDF-HFP mechanoluminescent composite film that
Highly sensitive detection of low-level water contents in. organic solvents and cyanide in aqueous media using novel. solvatochromic AIEE fluorophores
 Electronic Supplementary Material (ESI) for RSC Advances. This journal is The Royal Society of Chemistry 2015 Electronic Supplementary Information (ESI) Highly sensitive detection of low-level water contents
Electronic Supplementary Material (ESI) for RSC Advances. This journal is The Royal Society of Chemistry 2015 Electronic Supplementary Information (ESI) Highly sensitive detection of low-level water contents
Planar Pentacoordinate Carbon in CAl 5 + : A Global Minimum
 Supporting Information: Planar Pentacoordinate Carbon in CAl 5 + : A Global Minimum Yong Pei, Wei An, Keigo Ito, Paul von Ragué Schleyer, Xiao Cheng Zeng * Department of Chemistry and Nebraska Center for
Supporting Information: Planar Pentacoordinate Carbon in CAl 5 + : A Global Minimum Yong Pei, Wei An, Keigo Ito, Paul von Ragué Schleyer, Xiao Cheng Zeng * Department of Chemistry and Nebraska Center for
Two Spin-state Reactivity in the Activation and Cleavage of CO 2 by [ReO 2 ]
![Two Spin-state Reactivity in the Activation and Cleavage of CO 2 by [ReO 2 ] Two Spin-state Reactivity in the Activation and Cleavage of CO 2 by [ReO 2 ]](/thumbs/72/67566926.jpg) Page 1 of 22 vised Version: 5 May 2016 Submitted to: J. Phys. hem. Lett. Two Spin-state activity in the Activation and leavage of 2 by [ 2 ] Valentino anale, a-c, Robert Robinson Jr., d, Athanasios Zavras,
Page 1 of 22 vised Version: 5 May 2016 Submitted to: J. Phys. hem. Lett. Two Spin-state activity in the Activation and leavage of 2 by [ 2 ] Valentino anale, a-c, Robert Robinson Jr., d, Athanasios Zavras,
Ring expansion reactions of electron-rich boron-containing heterocycles. Supporting Information Contents
 Ring expansion reactions of electron-rich boron-containing heterocycles Juan. F. Araneda, Warren E. Piers,* Michael J. Sgro and Masood Parvez Department of Chemistry, University of Calgary, 2500 University
Ring expansion reactions of electron-rich boron-containing heterocycles Juan. F. Araneda, Warren E. Piers,* Michael J. Sgro and Masood Parvez Department of Chemistry, University of Calgary, 2500 University
Supporting Information
 Supporting Information The Catalytic Effect of Water, Formic Acid or Sulfuric Acid on the Reaction of Formaldehyde with OH Radicals Weichao Zhang *, Benni Du, Zhenglong Qin College of Chemistry and Chemical
Supporting Information The Catalytic Effect of Water, Formic Acid or Sulfuric Acid on the Reaction of Formaldehyde with OH Radicals Weichao Zhang *, Benni Du, Zhenglong Qin College of Chemistry and Chemical
Aluminum Siting in the ZSM-5 Framework by Combination of
 Supplementary Information Aluminum Siting in the ZSM-5 Framework by Combination of High Resolution 27 Al NMR and DFT/MM calculations Stepan Sklenak,* a Jiří Dědeček, a Chengbin Li, a Blanka Wichterlová,
Supplementary Information Aluminum Siting in the ZSM-5 Framework by Combination of High Resolution 27 Al NMR and DFT/MM calculations Stepan Sklenak,* a Jiří Dědeček, a Chengbin Li, a Blanka Wichterlová,
Metal-Free Hydrogenation Catalysis of Polycyclic Aromatic Hydrocarbons
 Supplementary Data for: Metal-Free Hydrogenation Catalysis of Polycyclic Aromatic Hydrocarbons Yasutomo Segawa b and Douglas W. Stephan* a a Department of Chemistry, University of Toronto, 80 St. George
Supplementary Data for: Metal-Free Hydrogenation Catalysis of Polycyclic Aromatic Hydrocarbons Yasutomo Segawa b and Douglas W. Stephan* a a Department of Chemistry, University of Toronto, 80 St. George
Supporting Material Biomimetic zinc chlorin poly(4-vinylpyridine) assemblies: doping level dependent emission-absorption regimes
 Supporting Material Biomimetic zinc chlorin poly(4-vinylpyridine) assemblies: doping level dependent emission-absorption regimes Ville Pale, a, Taru Nikkonen, b, Jaana Vapaavuori, c Mauri Kostiainen, c
Supporting Material Biomimetic zinc chlorin poly(4-vinylpyridine) assemblies: doping level dependent emission-absorption regimes Ville Pale, a, Taru Nikkonen, b, Jaana Vapaavuori, c Mauri Kostiainen, c
Ni II Tetrahydronorcorroles: Antiaromatic Porphyrinoids with Saturated Pyrrole Units
 Electronic Supplementary Material (ESI) for ChemComm. This journal is The Royal Society of Chemistry 206 Supporting Information Ni II Tetrahydronorcorroles: Antiaromatic Porphyrinoids with Saturated Pyrrole
Electronic Supplementary Material (ESI) for ChemComm. This journal is The Royal Society of Chemistry 206 Supporting Information Ni II Tetrahydronorcorroles: Antiaromatic Porphyrinoids with Saturated Pyrrole
Supporting Information
 Supporting Information Unimolecular Photoconversion of Multicolor Luminescence on Hierarchical Self-Assemblies Liangliang Zhu, Xin Li, Quan Zhang, Xing Ma, # Menghuan Li, # Huacheng Zhang, Zhong Luo, Hans
Supporting Information Unimolecular Photoconversion of Multicolor Luminescence on Hierarchical Self-Assemblies Liangliang Zhu, Xin Li, Quan Zhang, Xing Ma, # Menghuan Li, # Huacheng Zhang, Zhong Luo, Hans
Supporting Information
 Supporting Information The Contrasting Character of Early and Late Transition Metal Fluorides as Hydrogen Bond Acceptors Dan A. Smith,, Torsten Beweries, Clemens Blasius, Naseralla Jasim, Ruqia Nazir,
Supporting Information The Contrasting Character of Early and Late Transition Metal Fluorides as Hydrogen Bond Acceptors Dan A. Smith,, Torsten Beweries, Clemens Blasius, Naseralla Jasim, Ruqia Nazir,
Synergistic Effects of Water and SO 2 on Degradation of MIL-125 in the Presence of Acid Gases
 Supporting Information Synergistic Effects of Water and SO 2 on Degradation of MIL-125 in the Presence of Acid Gases William P. Mounfield, III, Chu Han,, Simon H. Pang, Uma Tumuluri, Yang Jiao, Souryadeep
Supporting Information Synergistic Effects of Water and SO 2 on Degradation of MIL-125 in the Presence of Acid Gases William P. Mounfield, III, Chu Han,, Simon H. Pang, Uma Tumuluri, Yang Jiao, Souryadeep
How Large is the Elephant in the Density Functional Theory Room?
 1 How Large is the Elephant in the Density Functional Theory Room? Frank Jensen Department of Chemistry, Aarhus University, Langelandsgade 140, DK-8000 Aarhus, Denmark A recent paper compares density functional
1 How Large is the Elephant in the Density Functional Theory Room? Frank Jensen Department of Chemistry, Aarhus University, Langelandsgade 140, DK-8000 Aarhus, Denmark A recent paper compares density functional
Motooka, Nishi, Fukuoka , Japan.
 Electronic Supplementary Information A highly luminescent spiro-anthracenone-based organic light-emitting diode through thermally activated delayed fluorescence Keiro Nasu, a Tetsuya Nakagawa, a Hiroko
Electronic Supplementary Information A highly luminescent spiro-anthracenone-based organic light-emitting diode through thermally activated delayed fluorescence Keiro Nasu, a Tetsuya Nakagawa, a Hiroko
A Fluorescent Heteroditopic Hemicryptophane Cage for the Selective Recognition of Choline Phosphate
 Electronic Supplementary Material (ESI) for ChemComm. This journal is The Royal Society of Chemistry 2014 A Fluorescent Heteroditopic Hemicryptophane Cage for the Selective Recognition of Choline Phosphate
Electronic Supplementary Material (ESI) for ChemComm. This journal is The Royal Society of Chemistry 2014 A Fluorescent Heteroditopic Hemicryptophane Cage for the Selective Recognition of Choline Phosphate
Supporting information for: Role of N7 protonation of guanine in determining structure, stability and function of RNA base pairs
 Electronic Supplementary Material (ESI) for Physical Chemistry Chemical Physics. This journal is the Owner Societies 2015 Supporting information for: Role of N7 protonation of guanine in determining structure,
Electronic Supplementary Material (ESI) for Physical Chemistry Chemical Physics. This journal is the Owner Societies 2015 Supporting information for: Role of N7 protonation of guanine in determining structure,
Supporting Information for
 Supporting Information for A permutation approach to the assignment of the configuration to diastereomeric tetrads by comparison of experimental and ab initio calculated differences in NMR data Przemysław
Supporting Information for A permutation approach to the assignment of the configuration to diastereomeric tetrads by comparison of experimental and ab initio calculated differences in NMR data Przemysław
Electronic Supplementary Information for:
 Electronic Supplementary Information for: Manipulating dynamics with chemical structure: Probing vibrationally-enhanced dynamics in photoexcited catechol Adam S. Chatterley, a,b Jamie D. Young, a Dave
Electronic Supplementary Information for: Manipulating dynamics with chemical structure: Probing vibrationally-enhanced dynamics in photoexcited catechol Adam S. Chatterley, a,b Jamie D. Young, a Dave
Ethynylene-linked Figure-eight. Octaphyrin( ): Synthesis and. Characterization of Its Two Oxidation States
 Supporting Information for Ethynylene-linked Figure-eight Octaphyrin(1.2.1.1.1.2.1.1): Synthesis and Characterization of Its Two Oxidation States Krushna Chandra Sahoo, Ϯ Marcin A. Majewski, Marcin Stępień,
Supporting Information for Ethynylene-linked Figure-eight Octaphyrin(1.2.1.1.1.2.1.1): Synthesis and Characterization of Its Two Oxidation States Krushna Chandra Sahoo, Ϯ Marcin A. Majewski, Marcin Stępień,
Atmospheric syn Vinyl Hydroperoxide Decay Mechanism. Austin Parsons and Liam Peebles (Kuwata; Macalester College)
 Atmospheric syn Vinyl Hydroperoxide Decay Mechanism Austin Parsons and Liam Peebles (Kuwata; Macalester College) Introduction Alkene ozonolysis is a major source of the atmospheric hydroxyl radical, which
Atmospheric syn Vinyl Hydroperoxide Decay Mechanism Austin Parsons and Liam Peebles (Kuwata; Macalester College) Introduction Alkene ozonolysis is a major source of the atmospheric hydroxyl radical, which
Supporting Information (SI)
 S1 Supporting Information (SI) Theoretical Study of Small Iron-oxyhydroxide Clusters and Formation of Ferrihydrite Bidisa Das, * Technical Research Centre (TRC). Indian Association for the Cultivation
S1 Supporting Information (SI) Theoretical Study of Small Iron-oxyhydroxide Clusters and Formation of Ferrihydrite Bidisa Das, * Technical Research Centre (TRC). Indian Association for the Cultivation
Decomposition!of!Malonic!Anhydrides. Charles L. Perrin,* Agnes Flach, and Marlon N. Manalo SUPPORTING INFORMATION
 S1 Decomposition!of!Malonic!Anhydrides Charles L. Perrin,* Agnes Flach, and Marlon N. Manalo SUPPORTING INFORMATION Complete Reference 26: M. J. Frisch, G. W. Trucks, H. B. Schlegel, G. E. Scuseria, M.
S1 Decomposition!of!Malonic!Anhydrides Charles L. Perrin,* Agnes Flach, and Marlon N. Manalo SUPPORTING INFORMATION Complete Reference 26: M. J. Frisch, G. W. Trucks, H. B. Schlegel, G. E. Scuseria, M.
Magnesium-mediated Nucleophilic Borylation of Carbonyl Electrophiles
 Supplementary Information for Magnesium-mediated Nucleophilic Borylation of Carbonyl Electrophiles Anne-Frédérique Pécharman, Michael S. Hill,* Claire L. McMullin* and Mary F. Mahon Department of Chemistry,
Supplementary Information for Magnesium-mediated Nucleophilic Borylation of Carbonyl Electrophiles Anne-Frédérique Pécharman, Michael S. Hill,* Claire L. McMullin* and Mary F. Mahon Department of Chemistry,
Speciation of Adsorbed Phosphate at Gold Electrodes: A Combined. Surface-Enhanced Infrared Absorption Spectroscopy and DFT Study
 Supporting information for Speciation of Adsorbed Phosphate at Gold Electrodes: A Combined Surface-Enhanced Infrared Absorption Spectroscopy and DFT Study Momo Yaguchi, 1,2 Taro Uchida, 3 Kenta Motobayashi,
Supporting information for Speciation of Adsorbed Phosphate at Gold Electrodes: A Combined Surface-Enhanced Infrared Absorption Spectroscopy and DFT Study Momo Yaguchi, 1,2 Taro Uchida, 3 Kenta Motobayashi,
Ionic liquid electrolytes for reversible magnesium electrochemistry
 Electronic Supplementary Material (ESI) for ChemComm. This journal is The Royal Society of Chemistry 2016 SUPPORTING INFORMATION Ionic liquid electrolytes for reversible magnesium electrochemistry Mega
Electronic Supplementary Material (ESI) for ChemComm. This journal is The Royal Society of Chemistry 2016 SUPPORTING INFORMATION Ionic liquid electrolytes for reversible magnesium electrochemistry Mega
Supporting Information
 Supporting Information Wiley-VCH 2007 69451 Weinheim, Germany From the alkyllithium aggregate [(nbuli) 2 PMDTA] 2 to lithiated PMDTA Carsten Strohmann*, Viktoria H. Gessner Institut für Anorganische Chemie,
Supporting Information Wiley-VCH 2007 69451 Weinheim, Germany From the alkyllithium aggregate [(nbuli) 2 PMDTA] 2 to lithiated PMDTA Carsten Strohmann*, Viktoria H. Gessner Institut für Anorganische Chemie,
Observation of Guanidine-Carbon Dioxide Complexation in Solution and Its Role in Reaction of Carbon Dioxide and Propargylamines
 Electronic Supplementary Material (ESI) for Catalysis Science & Technology. This journal is The Royal Society of Chemistry 2014 Observation of Guanidine-Carbon Dioxide Complexation in Solution and Its
Electronic Supplementary Material (ESI) for Catalysis Science & Technology. This journal is The Royal Society of Chemistry 2014 Observation of Guanidine-Carbon Dioxide Complexation in Solution and Its
Unveiling the role of hot charge-transfer states. in molecular aggregates via nonadiabatic. dynamics
 Unveiling the role of hot charge-transfer states in molecular aggregates via nonadiabatic dynamics Daniele Fazzi 1, Mario Barbatti 2, Walter Thiel 1 1 Max-Planck-Institut für Kohlenforschung Kaiser-Wilhelm-Platz
Unveiling the role of hot charge-transfer states in molecular aggregates via nonadiabatic dynamics Daniele Fazzi 1, Mario Barbatti 2, Walter Thiel 1 1 Max-Planck-Institut für Kohlenforschung Kaiser-Wilhelm-Platz
Electronic Supplementary Information (ESI)
 Electronic Supplementary Material (ESI) for RSC Advances. This journal is The Royal Society of Chemistry 0 Electronic Supplementary Information (ESI) Solar-energy-derived strained hydrocarbon as energetic
Electronic Supplementary Material (ESI) for RSC Advances. This journal is The Royal Society of Chemistry 0 Electronic Supplementary Information (ESI) Solar-energy-derived strained hydrocarbon as energetic
Methionine Ligand selectively promotes monofunctional adducts between Trans-EE platinum anticancer drug and Guanine DNA base
 Supplementary Material (ESI) for Chemical Communications This journal is The Royal Society of Chemistry 2010 Supplementary Information Methionine Ligand selectively promotes monofunctional adducts between
Supplementary Material (ESI) for Chemical Communications This journal is The Royal Society of Chemistry 2010 Supplementary Information Methionine Ligand selectively promotes monofunctional adducts between
SUPPORTING INFORMATION
 SUPPORTING INFORMATION Highly Luminescent Tetradentate Bis-Cyclometalated Platinum Complexes: Design, Synthesis, Structure, Photophysics, and Electroluminescence Application Dileep A. K. Vezzu, Joseph
SUPPORTING INFORMATION Highly Luminescent Tetradentate Bis-Cyclometalated Platinum Complexes: Design, Synthesis, Structure, Photophysics, and Electroluminescence Application Dileep A. K. Vezzu, Joseph
Supplemental Material
 Supplemental Material Sensitivity of Hydrogen Bonds of DNA and RNA to Hydration, as Gauged by 1 JNH Measurements in Ethanol Water Mixtures Marlon N. Manalo, Xiangming Kong, and Andy LiWang* Texas A&M University
Supplemental Material Sensitivity of Hydrogen Bonds of DNA and RNA to Hydration, as Gauged by 1 JNH Measurements in Ethanol Water Mixtures Marlon N. Manalo, Xiangming Kong, and Andy LiWang* Texas A&M University
Effect of Mono- and Di-hydration on the Intramolecular Proton Transfers and Stability of Cyanuric Acid Isomers: A DFT Study
 J. Chem. Sci. Vol. 128, No. 8, August 2016, pp. 1237 1244. c Indian Academy of Sciences. DOI 10.1007/s12039-016-1132-y Effect of Mono- and Di-hydration on the Intramolecular Proton Transfers and Stability
J. Chem. Sci. Vol. 128, No. 8, August 2016, pp. 1237 1244. c Indian Academy of Sciences. DOI 10.1007/s12039-016-1132-y Effect of Mono- and Di-hydration on the Intramolecular Proton Transfers and Stability
Infrared Spectra and Electronic Structure Calculations for the
 Supporting information: ic-2013-01233k Infrared Spectra and Electronic Structure Calculations for the NUN(NN) 1-5 and NU(NN) 1-6 Complexes in Solid Argon Lester Andrews,*Xuefeng Wang, and Yu Gong Department
Supporting information: ic-2013-01233k Infrared Spectra and Electronic Structure Calculations for the NUN(NN) 1-5 and NU(NN) 1-6 Complexes in Solid Argon Lester Andrews,*Xuefeng Wang, and Yu Gong Department
Supplementary Information. Institut für Anorganische Chemie, Julius-Maximilians Universität Würzburg, Am Hubland, D Würzburg, Germany.
 Electronic Supplementary Material (ESI) for ChemComm. This journal is The Royal Society of Chemistry 2014 Synthesis and Characterization of a Mercury-Containing Trimetalloboride Supplementary Information
Electronic Supplementary Material (ESI) for ChemComm. This journal is The Royal Society of Chemistry 2014 Synthesis and Characterization of a Mercury-Containing Trimetalloboride Supplementary Information
Supporting Information. Synthesis, resolution and absolute configuration of chiral 4,4 -bipyridines
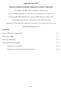 Supporting Information Synthesis, resolution and absolute configuration of chiral 4,4 -bipyridines Victor Mamane,* a Emmanuel Aubert, b Paola Peluso, c and Sergio Cossu d a Laboratoire SRSMC UMR CRS 7565,
Supporting Information Synthesis, resolution and absolute configuration of chiral 4,4 -bipyridines Victor Mamane,* a Emmanuel Aubert, b Paola Peluso, c and Sergio Cossu d a Laboratoire SRSMC UMR CRS 7565,
Supporting information
 Electronic Supplementary Material (ESI) for ChemComm. This journal is The Royal Society of Chemistry 2015 1 Supporting information Cryo-generated Ferrous-superoxo Porphyrin: EPR, Resonance Raman and DFT
Electronic Supplementary Material (ESI) for ChemComm. This journal is The Royal Society of Chemistry 2015 1 Supporting information Cryo-generated Ferrous-superoxo Porphyrin: EPR, Resonance Raman and DFT
Supporting Information. for. Silylation of Iron-Bound Carbon Monoxide. Affords a Terminal Fe Carbyne
 Supporting Information for Silylation of Iron-Bound Carbon Monoxide Affords a Terminal Fe Carbyne Yunho Lee and Jonas C. Peters* Division of Chemistry and Chemical Engineering, California Institute of
Supporting Information for Silylation of Iron-Bound Carbon Monoxide Affords a Terminal Fe Carbyne Yunho Lee and Jonas C. Peters* Division of Chemistry and Chemical Engineering, California Institute of
Synthesis, electrochemical and theoretical studies of. V-Shaped donor-acceptor hexaazatriphenylene. (HAT) derivatives for second harmonic generation
 Synthesis, electrochemical and theoretical studies of V-Shaped donor-acceptor hexaazatriphenylene (HAT) derivatives for second harmonic generation Rafael Juárez a, b, Mar Ramos a, José L. Segura b *, Jesús
Synthesis, electrochemical and theoretical studies of V-Shaped donor-acceptor hexaazatriphenylene (HAT) derivatives for second harmonic generation Rafael Juárez a, b, Mar Ramos a, José L. Segura b *, Jesús
Supporting Information for: Unusual para-substituent effects on the intramolecular hydrogen-bond in hydrazone-based switches
 Supporting Information for: Unusual para-substituent effects on the intramolecular hydrogen-bond in hydrazone-based switches Xin Su a, Märt Lõkov b, Agnes Kütt b, Ivo Leito b and Ivan Aprahamian a a Department
Supporting Information for: Unusual para-substituent effects on the intramolecular hydrogen-bond in hydrazone-based switches Xin Su a, Märt Lõkov b, Agnes Kütt b, Ivo Leito b and Ivan Aprahamian a a Department
A Key n π* Interaction in N-Acyl Homoserine Lactones
 A Key n π* Interaction in N-Acyl Homoserine Lactones Robert W. Newberry and Ronald T. Raines* Page Contents S1 Table of Contents S2 Experimental Procedures S3 Computational Procedures S4 Figure S1. 1 H
A Key n π* Interaction in N-Acyl Homoserine Lactones Robert W. Newberry and Ronald T. Raines* Page Contents S1 Table of Contents S2 Experimental Procedures S3 Computational Procedures S4 Figure S1. 1 H
SUPPORTING INFORMATION. In Search of Redox Noninnocence between a Tetrazine Pincer Ligand and Monovalent Copper
 Electronic Supplementary Material (ESI) for Dalton Transactions. This journal is The Royal Society of Chemistry 2014 SUPPORTING INFORMATION In Search of Redox Noninnocence between a Tetrazine Pincer Ligand
Electronic Supplementary Material (ESI) for Dalton Transactions. This journal is The Royal Society of Chemistry 2014 SUPPORTING INFORMATION In Search of Redox Noninnocence between a Tetrazine Pincer Ligand
Spin-Orbit Coupling, Spin-Spin, NMR and Electric Properties of Hydrogen Chloride Molecule
 ercrcrs craeser Spin-Orbit Coupling, Spin-Spin, NMR and Electric Properties of Hydrogen Chloride Molecule Dhia Hamdi Al-Amiedy 1, Zeyad Adnan Saleh 2, Rajaa Khedir Al-Yasari 3 1 Physics Department, College
ercrcrs craeser Spin-Orbit Coupling, Spin-Spin, NMR and Electric Properties of Hydrogen Chloride Molecule Dhia Hamdi Al-Amiedy 1, Zeyad Adnan Saleh 2, Rajaa Khedir Al-Yasari 3 1 Physics Department, College
